Dicloruro de metilfosfonilo
El dicloruro de metilfosfonilo (DC) o dicloro es un compuesto organofosforado. es usado como precursor de varios agentes de armas químicas. Es un sólido cristalino blanco que se funde ligeramente por encima de la temperatura ambiente.[2]
| Dicloruro de metilfosfonilo | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| Dicloruro de metilfosfonilo | ||
| General | ||
| Otros nombres |
Dicloruro de metanofosfónico Dicloruro de ácido metanofosfónico Dicloruro de metilfosfonilo Dicloro | |
| Fórmula estructural |
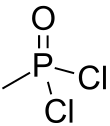 | |
| Fórmula molecular | CH3Cl2OP | |
| Identificadores | ||
| Número CAS | 676-97-1[1] | |
| ChemSpider | 12150 | |
| PubChem | 12671 | |
| UNII | 2XGZ22DHQ2 | |
|
CP(=O)(Cl)Cl
| ||
| Propiedades físicas | ||
| Apariencia | Sólido blanco cristalino | |
| Densidad | 1,468 kg/m³; 0,001468 g/cm³ | |
| Masa molar | 131,929857 g/mol | |
| Punto de fusión | 28 °C (301 K) °C a 34 °C (307 K) °C | |
| Punto de ebullición | 163 °C (436 K) °C | |
| Propiedades químicas | ||
| Solubilidad en agua | Reacciona con agua | |
| Solubilidad | Eter, THF | |
| Peligrosidad | ||
| SGA |
  | |
| Frases H | H314,H330 | |
| Frases P |
P260,P264,P271,P280,P284, P301+330+331,P303+361+353, P304+340,P305+351+338,P310, P320,P321,P363,P403+233, P405,P501 | |
| Riesgos | ||
| Riesgos principales | Muy tóxico, reacciona con agua | |
| LD50 | 26 ppm/4h por inalación (ratas) | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Síntesis y reacciones
editarEl dicloruro de metilfosfonilo se produce por oxidación de metildiclorofosfina con cloruro de sulfurilo:[3]
- CH3PCl2 + SO2Cl2 → CH3P(O)Cl2 + SOCl2
También se puede producir a partir de una gama de metilfosfonatos (por ejemplo, metilfosfonato de dimetilo) mediante cloración con cloruro de tionilo. Varias aminas catalizan este proceso.[4] Con fluoruro de hidrógeno o fluoruro de sodio, se puede utilizar para producir difluoruro de metilfosfonilo. Con alcoholes, se convierte en dialcóxido:[5]
- CH3P(O)Cl2 + 2 HOR → CH3P(O)(OR)2 + HCl
Seguridad
editarEl dicloruro de metilfosfonilo es muy tóxico y reacciona vigorosamente con el agua para liberar ácido clorhídrico. También figura en el Anexo 2 de la Convención sobre Armas Químicas, ya que se utiliza en la producción de agentes nerviosos organofosforados como el sarín y el somán.
Referencias
editar- ↑ Número CAS
- ↑ «SAFETY DATA SHEET Methylphosphonic dichloride». SAFETY DATA SHEET Methylphosphonic dichloride. MilliporeSigma. 26 de junio de 2020. Consultado el 27 de abril de 2022.
- ↑ Svara, J.; Weferling, N.; Hofmann, T. "Phosphorus Compounds, Organic," In 'Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2008. doi 10.1002/14356007.a19_545.pub2.
- ↑ Maier, Ludwig (1990). «Organic Phosphorus Compounds 90.l A Convenient, One-Step Synthesis of Alkyl- and Arylphosphonyl Dichlorides». Phosphorus, Sulfur, and Silicon and the Related Elements 47 (3–4): 465-470. doi:10.1080/10426509008038002.
- ↑ Carl Patois, Philippe Savignac, Elie About-Jaudet, Noël Collignon (1996). «Bis(Trifluoroethyl) (carboethoxymethyl)phosphonate». Organic Syntheses 73: 152. doi:10.15227/orgsyn.073.0152.