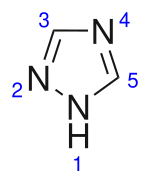
1,2,4-Triazol
El 1,2,4-triazol es uno de los 2 compuestos químicos isómeros con fórmula molecular C2H3N3 llamados triazoles, que tienen un anillo de cinco miembros de dos átomos de carbono y tres átomos de nitrógeno. El 1,2,4-triazol es un heterociclo aromático.[2]
| 1,2,4-Triazol | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| 1H-1,2,4-triazol | ||
| General | ||
| Otros nombres | 3,4-diazapirrol | |
| Fórmula estructural |
 | |
| Fórmula molecular | C2H3N3 | |
| Identificadores | ||
| Número CAS | 288-88-0[1] | |
| ChEMBL | CHEMBL15571 | |
| Propiedades físicas | ||
| Apariencia | sólido blanco | |
| Masa molar | 690 654 g/mol | |
| Punto de fusión | 120/−121 °C (393/152 K) | |
| Punto de ebullición | 260 °C (533 K) | |
| Propiedades químicas | ||
| Acidez | 2,2 pKa | |
| Alcalinidad | 10,3 pKb | |
| Solubilidad en agua | muy soluble | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Los derivados de 1,2,4-triazol encuentran su uso en una amplia variedad de aplicaciones, especialmente como antifúngicos tales como fluconazol, itraconazol, voriconazol, posaconazol, epoxiconazol, tebuconazol, flusilazol, paclobutrazol.
La estructura de este anillo aparece en ciertos carbenos N-heterocíclicos.
Propiedades
editarEl 1,2,4-triazol tiene dos tautómeros: el 1H y el 2-H:[3] como ocurría con su isómero el 1,2,3-triazol.
A altas temperaturas, el 1,2,4-triazol descompone a óxidos de nitrógeno, lo que explica su riesgo de explosión (punto de inflamación 170 °C, temperatura de ignición de 490 °C).
Síntesis
editarSe pueden sintetizar compuestos derivados de 1,2,4-triazol a través de la reacción de Pellizzari[4] o de la reacción de Einhorn-Brunner[5][6]
Referencias
editar- ↑ Número CAS
- ↑ Heterocyclic chemistry T.L. Gilchrist ISBN 0-582-01421-2
- ↑ Theophil Eicher, Siegfried Hauptmann, Andreas Speicher (2003). The Chemistry of Heterocycles: structure, reactions, syntheses, and applications. Wiley-VCH. ISBN 978-3-5273-0720-3.
- ↑ Potts K. T. (1961). «The Chemistry of 1,2,4-Triazoles.». Chemical Reviews 61 (2): 87-127. doi:10.1021/cr60210a001.
- ↑ Alfred Einhorn, Eduard Bischkopff, Bruno Szelinski, Gustav Schupp, Eduard Spröngerts, Carl Ladisch, Theodor Mauermayer (1905). «Ueber die N-Methylolverbindungen der Säureamide». Justus Liebig's Annalen der Chemie 343 (2-3): 207-305 (229). doi:10.1002/jlac.19053430207.
- ↑ Karl Brunner (1915). «Eine neue Darstellungsweise von Triazolen». Monatshefte für Chemie 36 (7-8): 509-534. doi:10.1007/BF01524682.