Tubocurarina
La tubocurarina (también conocida como d-tubocurarina o DTC) es un alcaloide bencilisoquinilínico tóxico que se encuentra en la planta Chondrodendron tomentosum conocido por su uso como veneno de flecha.
| Tubocurarina | ||
|---|---|---|
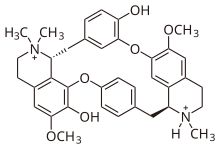 | ||
| Nombre (IUPAC) sistemático | ||
| 6,6'-dimetoxi-2,2,2',2'-tetrametiltubocuraran-2,2'-diium-7',12'-diol | ||
| Identificadores | ||
| Número CAS | 57-95-4 | |
| Código ATC | M03AA02 | |
| PubChem | 6000 | |
| Datos químicos | ||
| Fórmula | C37H42N2Cl2O6 | |
| Peso mol. | 624,765 g/mol | |
|
Oc7ccc1cc7Oc5cc6[C@H](Cc4ccc(Oc2c3[C@@H](C1)[N+](C)(C)CCc3cc(OC)c2O)cc4)[N+](C)(C)CCc6cc5OC
| ||
|
InChI=1S/C37H40N2O6/c1-38-14-12-24-19-32(42-4)33-21-27(24)28(38)16-22-6-9-26(10-7-22)44-37-35-25(20-34(43-5)36(37)41)13-15-39(2,3)29(35)17-23-8-11-30(40)31(18-23)45-33/h6-11,18-21,28-29H,12-17H2,1-5H3,(H-,40,41)/p+1/t28-,29+/m0/s1
| ||
| Farmacocinética | ||
| Vida media | 1-2 horas | |
| Datos clínicos | ||
| Estado legal | ? | |
| Vías de adm. | IV | |
A mediados del siglo XX, se usó como complemento de los anestésicos para provocar relajación del músculo esquelético durante la cirugía o la ventilación mecánica.
En la actualidad se utiliza raramente como complemento para la anestesia clínica debido a que están disponibles alternativas más seguras, como el cisatracurio y rocuronio. Actúa reduciendo la frecuencia de apertura del canal iónico acoplado al receptor nicotínico produciendo parálisis muscular.
Historia
editarSe sabe que en el siglo XV, los indígenas suramericanos de la cuenca del río Amazonas, lo usaban para envenenar las puntas de las flechas para la caza de los animales de consumo, ya que no afectaban a las personas que ingerían la carne. El veneno lo transportaban en tubos de bambú, de ahí el nombre de tubocurarina. A Europa llegó gracias a los escritos de Sir Walter Raleigh en el libro "Discovery of the Large, Rich and Beautiful Empire of Guiana". Alexander von Humboldt identificó en 1807 la Strychnos toxifera. Más tarde, se descubrieron otras especies del mismo y de distinto género que contenían sustancias tóxicas semejantes: Strychnos letalis, Chondodendron tomentosum (curare), Chondodendron platiphyllum y Erythrina americana.
Sir Benjamin Brodie fue el primero en advertir de los efectos paralizantes del curare en los músculos respiratorios. En 1812, experimentó con el curare y mostró que la ventilación artificial mantenía con vida a los animales curarizados. En 1825, Charles Waterton describió su experimento con curare en un asno inflando los pulmones del animal con un fuelle; de este modo lo mantuvo con vida artificialmente mientras el efecto del curare estuvo presente.
En 1850, Claude Bernard estableció las bases científicas de los relajantes musculares al mostrar la actuación del curare sobre la unión neuromuscular, bloqueando el impulso de los nervios motores. Inyectó curare en el saco linfático de la rana y observó un efecto paralizante del músculo, pero la conducción nerviosa estaba intacta y la estimulación eléctrica sobre el músculo no estaba alterada. Este experimento sirvió como base para descubrir que el efecto del bloqueo neuromuscular del curare ocurría en la placa motora terminal. En 1900, Jacob Pal descubrió que los anticolinesterásicos podían revertir la acción relajante del curare.
Rudolf Boehm aisló la curarina y el cirujano Arthur Läwen la utilizó por primera vez en anestesia, en 1912, para una cirugía abdominal utilizando ventilación. En 1935, King descubrió la estructura química de la d-tubocurarina. Un año después, West usó extractos purificados de estas plantas para el tratamiento de tres pacientes con tétanos. En 1941, el Laboratorio Squibb produjo una preparación de curare llamada “Intocostrin”. En 1942, Griffith y Johnson, usaron este medicamento en 25 pacientes para investigar los aspectos clínicos del curare. En 1947 Daniel Bovet obtuvo el primer derivado sintético que llamó gallamina. A esta siguieron pronto otros compuestos: el decametonio (1948). En 1949, Bovet sintetizó la succinilcolina y fue utilizada en clínica por primera vez en 1951 en varios países de Europa. En 1958 se describió el alcuronio, que fue utilizado en el hombre por primera vez en 1961; el pancuronio se sintetizó en 1964 y se usó clínicamente en 1966; el vecuronio fue introducido en 1979; el atracurio en 1980, el mivacurio en 1993 y el rocuronio en 1994.[1]
Propiedades químicas
editarEstructuralmente la tubocurarina es un derivado de la bencilisoquinolina. Durante muchos años, la estructura, cuando fue dilucidada en 1948,[2] se pensó erróneamente que era bis-cuaternaria: en otras palabras, se creía que era un alcaloide N,N-dimetilado. En 1970, se estableció la estructura correcta,[3] mostrando que uno de los dos nitrógenos era terciario, realmente un alcaloide mono-N-metilado.
Biosíntesis
editarLa biosíntesis de la tubocurarina involucra un acoplamiento radical de los dos enantiómeros de N-metil-coclaurina. (R) y (S)-N- metil-coclaurina viene de una reacción de semejante a la de Mannich entre la dopamina y la 4-hidroxifenil-acetaldehído, facilitado por la norcoclaurine sintasa (NCS). Tanto la dopamina y la 4-hidroxifenilacetiladehido se originan a partir de L-tirosina. La metilación de los sustituyentes amina e hidroxilo son facilitadas por S-adenosilmetionina (SAM).[4]
Farmacodinamica
editarMecanismo de acción
editarLa tubocurarina, a dosis terapéuticas, reduce la frecuencia de apertura del canal iónico acoplado al receptor sin afectar a otras propiedades, como la conductancia y el tiempo medio de apertura y, disminuyendo así, la amplitud del EPP. Si esta descendiese por debajo del 70 %, sería insuficiente para generar el potencial de acción, produciendo, de esta forma, la parálisis muscular característica de la tubocurarina.
El bloqueo neuromuscular causado se revierte tras el aumento de acetilcolina en la placa motriz, ya sea por la adición directa de esta o, indirectamente, por la administración de anticolinesterásicos, como la neostigmina. Todo ello sugiere un antagonismo de tipo competitivo.
Si se emplean concentraciones suficientemente elevadas de tubocurarina, el bloqueo neuromuscular no se revierte por la administración de anticolinesterásicos, sino que se agravaría. Ello se debe a que en esta situación la tubocurarina produciría un bloqueo del canal iónico similar al que producen algunos fármacos bloqueantes ganglionares.
Por todo ello, se comportaría además como un antagonista no competitivo.
Con las dosis empleadas en clínica de tubocurarina, sólo se observaría el bloqueo competitivo.
Todas estas acciones se realizan postsinápticamente. Sin embargo, también pueden actuar presinápticamente inhibiendo los receptores nicotínicos e impidiendo la liberación de acetilcolina durante la estimulación repetitiva de las terminaciones nerviosas. Esta acción puede ser responsable del decaimiento tetánico que se observa tras la administración.[5]
Efectos farmacológicos
editarSus efectos se deben principalmente a la parálisis muscular motora.
A dosis terapéutica por vía intravenosa, la instauración de los efectos es rápida y se observa una debilidad motora inicial que progresa a parálisis muscular. No todos los músculos se afectan con la misma rapidez: primeros los extrínsecos oculares y los faciales; la musculatura de las extremidades, del cuello y del tronco; músculos intercostales y el diafragma. Esto último conduce a la apnea. La recuperación sigue un orden inverso.
Una característica particular de estos compuestos es la reversión de sus efectos paralizantes por los anticolinesterásicos.
También ejercen acciones sobre otras estructuras: ganglios vegetativos, mastocitos y receptores muscarínicos.
También puede producir bloqueo de los receptores nicotínicos ganglionares, que puede agravarse por la acción adicional de la acetilcolina endógena sobre los receptores muscarínicos de los ganglios vegetativos, manifestándose como taquicardia e hipotensión.
También puede estimular la liberación de histamina de los mastocitos, lo que contribuye a la aparición de hipotensión, broncoespasmo en individuos sensibilizados (asmáticos) e hipersecreción salival y bronquial.[5]
Interacciones
editarLas interacciones se deben a la utilización de otros fármacos que también alteran la neurotransmisión de la placa motora, como antibióticos aminoglucósidos, produciendo un aumento de la intensidad del bloqueo sin que pueda verse revertido por los anticolinesterásicos; antagonistas del calcio, antiarrítmicos o anestésicos locales pueden potenciar también los efectos bloqueante neuromusculares; y los anestésicos inhalatorios que produce una potenciación de la intensidad y la duración del bloqueo.[6]
Farmacocinética
editarDebido a los grupos amonio cuaternario que contienen en su molécula, poseen una capacidad limitada de atravesar membranas. Por tanto, no se absorberían por vía oral. Este hecho era conocido por los indígenas que consumían con tranquilidad las piezas que cazaban utilizando curare.
Se absorben bien cuando se administran por vía intramuscular, no llegando al SNC, y su distribución es escasa. Se eliminan en buena parte sin modificar por el riñón.
La duración de acción de puede aumentar durante la anestesia debido a la depresión, tanto de las funciones renales o hepática, que se producen en los individuos con insuficiencia renal o hepática. Las características farmacocinéticas condicionan también el tiempo para alcanzar el efecto farmacológico.[7]
Efectos adversos
editarEl efecto adverso más importante es la parálisis respiratoria, a pesar de que este efecto disminuye por las condiciones de control de la respiración durante la anestesia.
Es mayor el peligro en el postoperatorio al haber restos de fármaco en el organismo, pudiendo ser potenciada por otros fármacos.
Debido al bloqueo, puede producir liberación de histamina, originando broncoespasmo, hipotensión y excesiva secreción bronquial y salival en personas sensibles.[7]
Aplicaciones terapéuticas
editarSe emplean en todas las situaciones que requieren relajación muscular intensa y relativamente prolongada. Su utilización principal es la inducción y el mantenimiento de la relajación muscular en intervenciones quirúrgicas.
Se emplea, de forma ocasional, para permitir una oxigenación adecuada en los pacientes de las unidades de cuidados intensivos, sobre todo en aquellos que presentan el síndrome de distrés respiratorio del adulto.
También permiten controlar algunos tipos de convulsiones, como las presentes en el tétanos o para facilitar la ventilación mecánica en otras situaciones en que esta es necesaria.
El advenimiento a la clínica de nuevos fármacos ha permitido mejorar notablemente la seguridad de su empleo y cada vez es menos frecuente el empleo de la tubocurarina.
Toxicidad
editarEl efecto letal de la d-tubocurarina se debe a la parálisis de los músculos esqueléticos, por el bloqueo selectivo de los receptores de acetilcolina, tanto en la sinapsis como en la placa neuromuscular. No afecta a la musculatura lisa o cardíaca, solamente al músculo estriado.
Muchas reacciones de toxicidad selectiva se basan en la inhibición competitiva con enzimas importantes en procesos fisiológicos como, por ejemplo, los productos organofosforados y carbámicos, que inhiben la acetilcolinesterasa; el fluoracetato, que interrumpe el ciclo de Krebs al bloquear el paso citrato-isocitrato por inhibición de la aconitasa; o el dicumarol con la vitamina K en los procesos hepáticos de síntesis de protrombina. Este proceso sería reversible si se administrase vitamina K.[8]
Referencias
editar- ↑ «Ariza de Arteaga, M. Unión neuromuscular y relajantes musculares. 2003. 01/11/2015.». Archivado desde el original el 17 de noviembre de 2015. Consultado el 15 de noviembre de 2015.
- ↑ King H (1948). «64. Curare alkaloids. Part VII. Constitution of dextrotubocurarine chloride». J Chem Soc: 265. doi:10.1039/jr9480000265.
- ↑ Everett AJ, Lowe LA, Wilkinson S (1970). J Chem Soc, Chem Commun: 1020.
- ↑ Dewick, P. M. Medicinal Natural Products; a Biosynthetic Approach. 3rd ed.; John Wiley and Sons Ltd.: 2009.
- ↑ a b Flores, J. Farmacología humana. 5.ª edición. Elsevier Masson, 2008.
- ↑ Katzung. B.G. Farmacología clínica y básica. 11.ª edición. Díaz de Santos, 2010.
- ↑ a b Velazquez- Farmacología básica y clínica. 18.ª edición. Panamérica, 2008.
- ↑ Repetto Kuhn, G. Toxicología fundamental. 4.ª edición. Mc Graw Hill, 2009.