Fosforilación oxidativa
La fosforilación oxidativa es un proceso metabólico que utiliza energía liberada por la oxidación de nutrientes para producir adenosina trifosfato (ATP). Se le llama así para distinguirla de otras rutas que producen ATP con menor rendimiento, llamadas "a nivel de sustrato". Se calcula que hasta el 90 % de la energía celular en forma de ATP es producida de esta forma.[1]
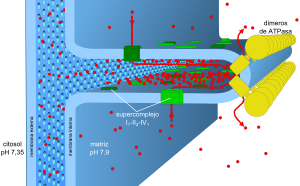
El modelo actual cubre algunos problemas suscitados por el anterior. En primer lugar, todos los componentes activos de la cadena de transporte de electrones se encuentran exclusivamente en las crestas mitocondriales y formando supercomplejos, en la imagen representado por el supercomplejo I1III2IV1. Esto permite canalizar de unos complejos a otros las moléculas de transferencia de electrones. Previamente se pensaba que difundían libremente. En segundo lugar, la diferencia de pH, uno de los componentes de la fuerza protón-motriz junto con el potencial de membrana (ΔΨ) es de tan sólo 0,55 unidades, equivalente a 32 mV, insuficiente para impulsar la fosforilación. Sin embargo, existen circunstancias locales que aumentan este pH en un factor de 2 unidades. En primer lugar, la ATP sintasa forma dímeros y filas que comban y dan forma a la cresta mitocondrial, haciendo que el espacio interno tenga tan sólo 20 ± 4 nm. El espacio entre la membrana interna y externa es menor, de 12 ± 2,5 nm, pero cuenta con poros lo suficientemente grandes como para estar en equilibrio con el citoplasma. Los protones se concentran gracias al «efecto superficie» y al rápido flujo desde las fuentes de protones a los sumideros. :V
Consta de dos etapas: en la primera, la energía libre generada mediante reacciones químicas redox en varios complejos multiproteicos —conocidos en su conjunto como cadena de transporte de electrones— se emplea para producir, por diversos procedimientos como bombeo, ciclos quinona/quinol o bucles redox, un gradiente electroquímico de protones a través de una membrana asociada en un proceso llamado quimiosmosis. La cadena respiratoria está formada por tres complejos de proteínas principales (complejo I, III, IV), y varios complejos «auxiliares», utilizando una variedad de donantes y aceptores de electrones. Los tres complejos se asocian en supercomplejos para canalizar las moléculas transportadoras de electrones, la coenzima Q y el citocromo c, haciendo más eficiente el proceso.
La energía potencial de ese gradiente, llamada fuerza protón-motriz, se libera cuando se translocan los protones a través de un canal pasivo, la enzima ATP sintasa, y se utiliza en la adición de un grupo fosfato a una molécula de ADP para almacenar parte de esa energía potencial en los enlaces anhidro «de alta energía» de la molécula de ATP mediante un mecanismo en el que interviene la rotación de una parte de la enzima a medida que fluyen los protones a través de ella. En vertebrados, y posiblemente en todo el reino animal, se genera un ATP por cada 2,7 protones translocados. Algunos organismos tienen ATPasas con un rendimiento menor.
Existen también proteínas desacopladoras que permiten controlar el flujo de protones y generar calor desacoplando ambas fases de la fosforilación oxidativa.
Aunque las diversas formas de vida utilizan una gran variedad de nutrientes, casi todas realizan la fosforilación oxidativa para producir ATP, la molécula que provee de energía al metabolismo. Esta ruta es tan ubicua debido a que es una forma altamente eficaz de liberación de energía, en comparación con los procesos alternativos de fermentación, como la glucólisis anaeróbica.
Pese a que la fosforilación oxidativa es una parte vital del metabolismo, produce una pequeña proporción de especies reactivas del oxígeno tales como superóxido y peróxido de hidrógeno, lo que lleva a la propagación de radicales libres, provocando daño celular, contribuyendo a enfermedades y, posiblemente, al envejecimiento. Sin embargo, los radicales tienen un importante papel en la señalización celular, y posiblemente en la formación de enlaces disulfuro de las propias proteínas de la membrana interna mitocondrial. Las enzimas que llevan a cabo esta ruta metabólica son blanco de muchas drogas y productos tóxicos que inhiben su actividad.
Historia
editarEl estudio de la fosforilación oxidativa se inició en 1906 con el informe de Arthur Harden sobre el papel vital del fosfato en la fermentación celular, aunque inicialmente se pensaba que solo los azúcar-fosfato estaban involucrados.[2] Sin embargo, a principios de los años 1940, la relación entre la oxidación de los azúcares y la generación de ATP fue establecida de forma definitiva por Herman Kalckar,[3] confirmando el papel central del ATP en la transferencia de energía, que había sido propuesto por Fritz Albert Lipmann en 1941.[4] Más tarde, en 1949, Friedkin y Morris Albert L. Lehninger demostraron que la coenzima NADH se encuentra relacionada con vías metabólicas tales como el ciclo del ácido cítrico y la síntesis de ATP.[5]
Durante otros veinte años, el mecanismo por el cual se generaba el ATP siguió siendo un misterio, con científicos buscando un elusivo «intermediario de alta energía», que enlazara las reacciones de oxidación y fosforilación.[6] El misterio fue resuelto por Peter D. Mitchell con la publicación de la teoría quimiosmótica en 1961.[7] En un principio la propuesta fue muy controvertida, pero fue aceptada lentamente y finalmente Mitchell recibió el Premio Nobel de Química en 1978 por su teoría.[8][9] La investigación posterior se centró en la purificación y caracterización de las enzimas involucradas, con importantes contribuciones realizadas por David E. Green sobre los complejos de la cadena de transporte de electrones, así como de Efraim Racker sobre la ATP sintasa.[10] Un paso fundamental hacia la solución de los mecanismos de la ATP sintasa fue proporcionada por Paul D. Boyer, con su desarrollo en 1973 del mecanismo de «cambio de unión», seguido por su radical propuesta de un sistema de catálisis rotacional en 1982.[11][12] Los trabajos más recientes incluyen estudios estructurales de las enzimas involucradas en la fosforilación oxidativa, llevados a cabo por John E. Walker, habiendo obtenido Walker y Boyer el Premio Nobel en 1997.[13]
Transferencia de energía por quimiosmosis
editarLa fosforilación oxidativa funciona con dos tipos de reacciones que están acopladas, una utiliza reacciones químicas que liberan energía, mientras que la otra utiliza esa energía para llevar a cabo sus reacciones.[14] El flujo de electrones a través de la cadena de transporte de electrones, desde donantes de electrones como NADH a aceptores de electrones tales como oxígeno, es un proceso exergónico —libera energía—, mientras que la síntesis de ATP es un proceso endergónico, el cual requiere de energía. Tanto la cadena de transporte de electrones como la ATP sintasa, están embebidos en la membrana, y la energía es transferida de la cadena de transporte de electrones a la ATP sintasa por el movimiento de protones a través de la membrana, en un proceso llamado quimiosmosis.[15] En la práctica, se comporta de manera similar a un simple circuito eléctrico, con una corriente de protones siendo transportados desde el lado negativo, lado N de la membrana hacia el lado positivo, lado P, por las enzimas de la cadena de transporte de electrones que bombean protones. Estas enzimas son como una batería, ya que realizan trabajo, para llevar corriente a través del circuito. El movimiento de protones crea un gradiente electroquímico a través de la membrana, el cual es llamado generalmente fuerza protón-motriz. Este gradiente tiene dos componentes: una diferencia en la concentración de protones (un gradiente de pH) y una diferencia en el potencial eléctrico, con un lado N, que posee carga negativa. La energía es almacenada mayormente como la diferencia de potenciales eléctricos en la mitocondria, pero también como un gradiente de pH en los cloroplastos.[16]
La ATP sintasa libera esta energía almacenada completando el circuito y permitiendo a los protones fluir a través del gradiente electroquímico, de nuevo hacia el lado N de la membrana.[17] Esta enzima se comporta de manera similar a un motor eléctrico ya que utiliza la fuerza protón-motriz para llevar a cabo la rotación de parte de su estructura y acoplar este movimiento con la síntesis de ATP.
La cantidad de energía liberada por la fosforilación oxidativa es elevada, comparada con la cantidad producida por la fermentación anaeróbica. La glucólisis produce solo dos moléculas de ATP, en cambio entre 30 y 36 ATP son producidos por la fosforilación oxidativa de los 10 NADH y 2 succinato obtenidos a través de la conversión de una molécula de glucosa en dióxido de carbono y agua.[18] Este resultado de ATP es el máximo teórico, ya que en la práctica algunos protones se filtran a través de la membrana, disminuyendo así la producción de ATP.[19]
Moléculas de transferencia de protones y electrones
editarLa cadena de transporte de electrones transporta tanto protones como electrones, transfiriendo electrones desde donantes hacia aceptores, y transportando protones a través de la membrana. Estos procesos utilizan moléculas de transferencia tanto solubles como unidas a proteínas. En la mitocondria, los electrones son transferidos dentro del espacio intermembranal por la proteína de transferencia de electrones solubles en agua, citocromo c.[20] Esto transporta solamente electrones, y estos son transferidos por la reducción y oxidación de un átomo de hierro que se encuentre en el grupo hemo de la proteína. El citocromo c se encuentra también en algunas bacterias, donde se ubica en el espacio periplasmático.[21]
Dentro de la membrana interna mitocondrial, el transportador de electrones liposoluble, la coenzima Q10 (Q) transporta tanto electrones como protones a través de un ciclo redox.[22] Esta pequeña molécula de benzoquinona es muy hidrófobica, de modo que difunde libremente en la membrana. Cuando Q acepta dos electrones o libera dos protones, es reducida a su forma ubiquinol (QH2); cuando QH2 libera dos electrones o acepta dos protones, es oxidada a su forma original de ubiquinona (Q). Como resultado, si dos enzimas están organizadas de modo que Q es reducida de un lado de la membrana y QH2 oxidada en el otro, la ubiquinona se acoplará a estas reacciones y actuará como lanzadera de protones a través de la membrana.[23] Algunas cadenas de transporte de electrones bacterianas utilizan quinonas diferentes, como la menaquinona, aparte de la ubiquinona.[24]
Dentro de las proteínas, los electrones son transferidos entre cofactores de flavina,[17][25] centros hierro-azufre, y citocromos. Existen varios tipos de centros hierro-azufre; los más simples que se encuentran en la cadena de transferencia de electrones consisten en dos átomos de hierro unidos por dos átomos azufre inorgánico; estos son centros [2Fe–2S]. El segundo tipo, los centros [4Fe–4S], contienen un cubo de cuatro átomos de hierro y cuatro de azufre. Cada átomo de hierro en estos centros es coordinado por un aminoácido, generalmente por el átomo de azufre de la cisteína. Los iones metálicos cofactores atraviesan por reacciones redox sin unir o liberar protones, de modo que en la cadena de transporte de electrones sirven solamente para el transporte de electrones entre proteínas. Los electrones se desplazan largas distancias a través de las proteínas saltando entre las cadenas que forman estos cofactores.[26] Esto ocurre por efecto túnel, el cual es rápido sobre distancias menores a 1,4−9 m.[27]
Cadena de transporte de electrones en eucariotas
editarMuchos procesos bioquímicos catabólicos, tales como la glucólisis, el ciclo de Krebs y la beta oxidación, producen la coenzima reducida NADH. Esta coenzima contiene electrones que tiene un elevado potencial de transferencia; es decir, que liberan una gran cantidad de energía tras su oxidación. Sin embargo, la célula no libera toda esta energía a la vez, si no sería una reacción incontrolable. En vez de ello, los electrones son eliminados del NADH y transferidos al oxígeno a través de una serie de enzimas cada una de las cuales libera una pequeña cantidad de energía. Este conjunto de enzimas, que consiste en complejos, del I al IV, llamado cadena de transporte de electrones se encuentra en la membrana de la mitocondria. El succinato también es oxidado por la cadena de transporte de electrones, pero entra en la vía metabólica por un punto diferente.
En eucariotas, las enzimas en este sistema de transporte de electrones utilizan la energía liberada de la oxidación de NADH para bombear protones a través de la membrana interna mitocondrial. Esto provoca una acumulación de protones en el espacio intermembrana, y genera un gradiente electroquímico a través de la membrana. La energía almacenada en este potencial es luego utilizada por la ATP sintasa para producir ATP. La fosforilación oxidativa en las mitocondrias de organismos eucariotas es el ejemplo de este proceso mejor comprendido. Las mitocondrias están presentes en casi todos los eucariotas, con la excepción de los protozoarios anaeróbicos tales como Trichomonas vaginalis que en su lugar reducen protones a hidrógeno en una reminiscencia de mitocondria llamada hidrogenosoma.[28]
Se ha comprobado que las enzimas de la cadena respiratoria se sitúan preferentemente en la membrana de las crestas mitocondriales. La membrana crestal está enriquecida en los componentes de estos complejos, aproximadamente en un 70 % del total. Se ha sugerido que esta distribución asimétrica podría deberse a que las juntas crestales suponen una barrera dinámica.[29]
| Enzima respiratoria | Par redox | Potencial medio
(Volts) |
|---|---|---|
| NADH deshidrogenasa | NAD+ / NADH | −0,32[30] |
| Succinato deshidrogenasa | FMN o FAD / FMNH2 o FADH2 | −0,20[30] |
| Complejo del citocromo bc1 | Coenzima Q10ox / Coenzima Q10red | +0,06[30] |
| Complejo del citocromo bc1 | Citocromo box / Citocromo bred | +0,12[30] |
| Complejo IV | Citocromo cox / Citocromo cred | +0,22[30] |
| Complejo IV | Citocromo aox / Citocromo ared | +0,29[30] |
| Complejo IV | O2 / HO- | +0,82[30] |
| Condiciones: pH = 7[30] | ||
NADH- ubiquinona oxidorreductasa (complejo I)
editarLa NADH-ubiquinona oxidorreductasa, también conocida como NADH deshidrogenasa o complejo I, es el primer complejo proteico en la cadena de transporte de electrones. Es uno de ensamblajes enzimáticos de membrana de mayor tamaño, y el mayor de la cadena respiratoria.
En términos generales, la reacción que cataliza es la oxidación de NADH y la transferencia de dos electrones a una quinona, normalmente una ubiquinona de entre 8 y 10 isoprenilos, aunque admite varios sustratos análogos. Posteriormente utiliza la energía liberada en esta reacción para la translocación de cuatro protones desde la matriz al espacio de intermembrana. La existencia de complejos I translocadores de Na+, aunque ha sido postulado en procariotas, hoy en día no se sustenta en la evidencia.[31] En bacterias marinas y patógenas, como Vibrio cholerae existe una enzima diferente y sin aparente homología, la NADH:Ubiquinona oxidoreductasa dependiente de sodio, que bombea un ion Na+ por electrón en lugar protones.[32]
La ecuación global de esta reacción es:
Esta reacción tiene dos componentes termodinámicamente distintos: Uno muy favorable, la transferencia de dos electrones desde NADH hasta la quinona. Los siguientes parámetros para las correspondientes semirreacciones pueden variar por las condiciones de solución, de membrana y de la posición de la cabeza de la quinona dentro de ella:
Lo cual nos da un
Mecanismo catalítico de la reacción red/ox
editarLa reacción global de oxidación de la quinona por NADH tiene lugar a una velocidad elevadísima (Kcat≈500 s-1). La cinética y el mecanismo catalítico concreto se infieren de varios estudios, de tipo estructural a partir de la cristalografía de rayos X del complejo I de T. termophilus y de estudios de EPR a muy bajas temperaturas, conocida como "freeze quenching".[34] La longitud que recorren los electrones desde el centro de unión a flavina hasta el último centro, el N2 es de unos 90 Å. El primer paso consiste en la transferencia de dos electrones desde el NADH a la Flavina mononucleótido en la subunidad NDFUV1. Aunque no está probado, parece ser que lo más probable es que esto suceda mediante transferencia del hidruro, (o sea, dos electrones y un protón) evitando de esa manera la formación del intermediario NAD., que es inestable. Los estudios estructurales en T. thermophilus avalan esta posibilidad. Para ello, el NADH "apilaría" su anillo nicotinamida sobre el anillo isoaloxazina de la flavina, siendo el carbono C4 el donante de electrones en el NADH, y el aceptor sería el Carbono C5 de la flavina, separados ambos una distancia de unos 3,5 Å. En B.Taurus, a PH=7,8, los potenciales de NAD+ (-0,35 V) y de la flavina (-0,38 V)son muy próximos, de modo que este paso es reversible. Su velocidad es muy elevada: El proceso de unión de NADH, transferencia del hidrido y liberación de NAD+ tiene una KcatNADH/KmNADH>1 x 107 M-1 s-1[35] Es decir, que tiene lugar en un tiempo menor de 90 μs, lo cual está por debajo de la capacidad de medición de los instrumentos actuales más precisos.[34]
El segundo paso es muy importante, porque los dos electrones no son transferidos simultáneamente a la quinona: Uno de ellos pasa a gran velocidad (≈90μs) por toda la cadena de centros [Fe-S] hacia el último de ellos, el N2, próximo a la quinona, mientras que el otro es transferido a un centro próximo a la flavina (12 Å), el N1a y a la misma velocidad, por lo que se supone que ambos centros tienen el máximo potencial reductor de toda la enzima. Una vez oxidados ambos centros, la enzima parece "pararse" 1ms, lo cual parece indicar que ese es el periodo en el que la enzima aún permanece ligada al NAD+ para evitar la entrada de un nuevo NADH. Dado que el centro más cercano es el N3, y está en la vía de N2, es muy probable que el primero de los electrones parta hacia este centro, dejando durante un breve instante a la flavina como un intermediario flavosemiquinona. A partir de ahí, el electrón que entra en N3 parte hacia los centros N1b, N4 y N5. Todos ellos tienen un potencial redox muy similar, de modo que el electrón estaría "equilibrado" moviéndose entre ellos. La velocidad a la que tiene lugar la transmisión desde el paso limitante, es decir, el más lento (que o bien es la oxidación del NADH o la reducción de FMN) hasta la quinona avala la idea de que esto se produce por efecto túnel, unido a que todos los centros, salvo el N7 se encuentran por debajo de la distancia limitante de 14 Å.[36]
Lo cierto es que durante el tiempo que la enzima aparentemente permanece unida al NAD<+, no se detectan apenas señales del intermediario ubisemiquinona, lo cual significa que no es transferido a la semiquinona, y tampoco se detecta una caída significativa de energía libre. Se han propuesto varias explicaciones: El segundo electrón sería "retenido" en el centro N1a para evitar que se forme el intermediario flavosemiquinona, que podría generar radicales superóxido, puesto que este centro es fácilmente accesible al oxígeno. Entre tanto, el segundo electrón generaría un cambio conformacional suficiente para que pueda pasar el segundo y de esa manera ser transferidos casi simultáneamente a la quinona. En este momento se detecta el descenso en la energía libre.[36] El lugar donde se une la quinona, entre las subunidades hidrofóbica e hidrofílica parece tener la suficiente holgura para aceptar una gran variedad de bloqueantes.[37]
Este sistema también puede producir radicales superóxido, pero la cantidad y los lugares donde se producen, así como los mecanismos y proporciones concretas son objeto de mucha controversia y problemas de interpretación; aunque deben ser elevados, se discuten las cifras de 1-4 % del oxígeno respirado para todo el sistema OXPHOS.[38]
Estructura funcional
editarHasta el momento no se tenían datos completos de cristalografía de rayos X del complejo con resolución suficiente, pero recientemente se ha podido lograr un modelo para la bacteria Thermus thermofilus de entre 3,3-4 Å, con lo que se están esclareciendo algunos detalles del mecanismo catalítico que eran desconocidos.[37]
En mitocondrias bovinas es un heteromultímero que consta de 45 subunidades, con una masa molecular de 969 kilodaltons (kDa).[39][40][41] En procariotas su tamaño es menor, y típicamente está formada por 14 subunidades y 10 cofactores, con un tamaño aproximado de 550 KDa.[42] Todas ellas cuentan homólogos en la forma mitocondrial, y se cree que forman la llamada "enzima mínima" o nuclear, ya que se considera que son suficientes para la transducción energética.[43] En plantas y algas el número de subunidades totales es 30, y en hongos, 37.[44] Recientemente un análisis ha encontrado homólogos de tres de estas proteínas supernumerarias en el complejo I de α-proteobacterias, consideradas las antepasadas de las mitocondrias.[45]
El resto de subunidades del complejo I mitocondrial, llamadas «accesorias», o «supernumerarias», varía en su número según las especies, tienen funciones enzimáticas aparentemente no relacionadas con la transducción energética, y su función no se comprende completamente.[46] Las siete subunidades "nucleares" del dominio intrínseco o de membrana son codificadas por el genoma mitocondrial, mientras que el resto lo son por el genoma nuclear. El ensamblaje de la enzima es muy complejo y no conocido en su totalidad, produciéndose patologías si surgen defectos.[47]
El complejo, que tiene forma de "L" consta de dos partes: una hidrofílica o extrínseca, que mira a la matriz o "lado P" de la membrana, y otra embebida en la propia membrana, llamada porción hidrofóbica o intrínseca. Las siete proteínas "nucleares" codificadas por el genoma mitocondrial se encuentran todas en esta porción. La enzima bovina, cuando se purifica en presencia de agentes caotrópicos suaves, puede disociarse en cuatro subcomplejos según las condiciones de tratamiento: Iα que comprende toda la porción extrínseca (Iλ) y parte de la intrínseca (Iγ) y la parte Iβ, que comprende casi toda la parte intrínseca. Funcionalmente consta de tres módulos: el módulo N, que une NADH y captura sus electrones transmitiéndolos al FMN y contiene los dos grupos prostéticos [2Fe-2S], el módulo Q, que contiene el resto de centros hierro sulfuro y transfiere esos electrones a la quinona, y por último el módulo P, encargado del bombeo de protones.[47]
Regulación
editarLa regulación de la actividad del complejo I se produce principalmente por tres mecanismos: Control de la expresión génica, integración en supercomplejos ("respirasomas") e interacciones con otras proteínas, en especial, modificaciones postaduccionales.[39]
Complejos auxiliares
editarLos complejos auxiliares de la cadena respiratoria son un grupo de complejos multiproteicos que realizan la transferencia de electrones sin bombear protones al espacio de intermembrana. En la mayoría de los casos ello se debe a que el potencial de reducción de sus sustratos está muy próximo al de las quinonas y es insuficiente para la translocación de protones. También se consideran dentro de este grupo las llamadas "oxidasas alternativas", que transfieren electrones al oxígeno sin pasar por el complejo III y la citocromo oxidasa (complejo IV).[48]
Succinato-Q oxidorreductasa (complejo II)
editarLa enzima succinato-Q oxidorreductasa, también conocida como complejo II o sucinato deshidrogenasa, es el segundo punto de entrada en la cadena de transporte de electrones.[49] Es inusual debido a que esta enzima es la única que forma parte de los procesos del ciclo de Krebs y de la cadena de transporte de electrones. El complejo II consiste en cuatro subunidades de proteínas y contiene unida como cofactor la flavín adenín dinucleótido (FAD), centros hierro-azufre, y un grupo hemo que no participa en la transferencia de electrones hacia la coenzima Q, pero que se cree es importante en disminuir la producción de especies reactivas del oxígeno.[50][51] Oxida el succinato a fumarato y reduce la ubiquinona. Debido a que esta reacción libera menos energía que la oxidación de NADH, el complejo II no transporta electrones a través de la membrana y no contribuye al gradiente de protones.
En algunos eucariotas, tales como el helminto Ascaris suum, una enzima similar al complejo II, fumarato reductasa (menaquinol:fumarato oxidorreductasa, o QFR), opera de forma reversa oxidando ubiquinol y reduciendo fumarato. Esto permite al helminto sobrevivir en el ambiente anaeróbico del intestino grueso, llevando a cabo una fosforilación oxidativa anaeróbica con fumarato como aceptor de electrones.[52] Otra función no convencional del complejo II es observada en el parásito que provoca la malaria Plasmodium falciparum. En este caso, la acción invertida del complejo II como oxidasa es importante para regenerar el ubiquinol, el cual el parásito utiliza como una forma inusual de biosíntesis de pirimidina.[53]
Flavoproteína de transporte de electrones Q oxidorreductasa
editarLa flavoproteína de transporte de electrones ubiquinona oxidorreductasa (oxidorreductasa ETF-Q), también conocida como flavoproteína de transporte de electrones deshidrogenasa, es el tercer punto de entrada a la cadena de transporte de electrones. Es una enzima que acepta electrones de la flavoproteína de transferencia de electrones en la matriz mitocondrial, y utiliza estos electrones para reducir ubiquinona.[54] Esta enzima contiene una flavina y un centro [4Fe–4S], pero, a diferencia de otros complejos respiratorios, se une a la superficie de la membrana y no atraviesa la bicapa lipídica.[55]
En mamíferos, esta ruta metabólica es importante en la beta oxidación de ácidos grasos y el catabolismo de aminoácidos y colinas, al aceptar electrones de múltiples acetil-CoA deshidrogenasas.[56][57] En plantas, la oxidorreductasa ETF-Q también es importante en la respuesta que permite la supervivencia por extensos periodos de oscuridad.[58]
Reductasas y oxidasas alternativas
editarMuchos organismos eucariotas poseen cadenas de transporte de electrones diferentes a la de los mamíferos, que difieren mucho de las más estudiadas de estos últimos (descritas anteriormente). Por ejemplo, en plantas, existen NADH oxidasas que oxidan el NADH en el citosol en lugar de la matriz mitocondrial, y transfieren estos electrones a las reservas de ubiquinona.[59] Estas enzimas no transportan protones, y por ello, reducen ubiquinona sin alterar el gradiente electroquímico a través de la membrana interna.[60]
Otro ejemplo de cadena de transporte de electrones divergente es la oxidasa alternativa, que es encontrada en plantas, así como algunos hongos, protistas y posiblemente algunos animales.[61][62] Esta enzima transfiere electrones directamente del ubiquinol al oxígeno.[63]
Las rutas de transporte de electrones producidos por estas oxidasas alternativas de NADH y ubiquinona tienen un menor rendimiento de ATP que la ruta completa. Las ventajas que se obtienen por estas rutas más cortas no son del todo conocidas. Sin embargo, las oxidasas alternativas son producidas como respuesta a situaciones de estrés ambiental, como el frío, especies reactivas del oxígeno e infección por patógenos, así como otros factores que inhiben la cadena de transporte de electrones completa.[64][65] Las rutas alternativas podrían, por lo tanto, aumentar la resistencia de los organismos ante daños, reduciendo el estrés oxidativo.[66]
Q-citocromo c oxidorreductasa (complejo III)
editarLa Q-citocromo c oxidorreductasa también conocida como citocromo c reductasa, complejo del citocromo bc1, o simplemente complejo III.[67][68] En mamíferos, esta enzima es un dímero, con cada subunidad del complejo conteniendo once subunidades de proteínas, un centro hierro-azufre [2Fe-2S] y tres citocromos: un citocromo c1 y dos citocromos b.[69] Un citocromo es un tipo de proteína de transferencia de electrones que contiene al menos un grupo hemo. Los átomos de hierro dentro del grupo hemo del complejo III alternan entre sus estados de oxidación reducido (+2) y oxidado (+3) mientras los electrones son transferidos a través de la proteína.
La reacción catalizada por el complejo III es la oxidación de una molécula de ubiquinol y la reducción de dos moléculas de citocromo c, una proteína hemo libremente asociada con la mitocondria. A diferencia de la coenzima Q, que transporta dos electrones, el citocromo c transporta solo uno.
Debido a que solo uno de los electrones puede ser transferido desde el donante QH2 al aceptor citocromo c, a la vez, el mecanismo de reacción del complejo III es más elaborado que aquellos de los otros complejos respiratorios, y se da en dos pasos, llamados ciclo Q.[70] En el primer paso, la enzima se une a tres sustratos, primero, QH2, el cual es luego oxidado, siendo un electrón transferido al segundo sustrato, el citocromo c. Los dos protones liberados de QH2 pasan al espacio intermembrana. El tercer sustrato es Q, el cual acepta el segundo electrón de QH2 y es reducido a Q.-, el cual es un radical libre de ubisemiquinona. Los primeros dos sustratos son liberados, pero este intermediario de ubisemiquinona permanece unido. En el segundo paso, una segunda molécula de QH2 es unida y de nuevo pasa su primer electrón al aceptor citocromo c. El segundo electrón es transferido a la ubisemiquinona unida, reduciéndola a QH2 mientras gana dos protones de la matriz mitocondrial. Este QH2 es luego liberado de la enzima.[71]
Como la coenzima Q es reducida a ubiquinol en el lado interno de la membrana y oxidado a ubiquinona en el externo, hay una transferencia neta de electrones a través de la membrana, añadidos al gradiente de protones.[17] El mecanismo más bien complejo de dos pasos por el cual sucede esto es importante, ya que incrementa la eficiencia de la transferencia de protones. Si, en lugar del ciclo Q, una molécula de QH2 fuese utilizada directamente para reducir dos moléculas del citocromo c, la eficiencia se reduciría a la mitad, siendo transferido solo un protón por citocromo c reducido.[17]
Citocromo c oxidasa (complejo IV)
editarLa citocromo c oxidasa, también conocida como complejo IV, es el complejo final de proteínas en la cadena de transporte de electrones.[72] En mamíferos esta enzima posee una estructura extremadamente compleja y contiene trece subunidades, dos grupos hemo, así como múltiples iones metálicos como cofactores – en todas, tres átomos de cobre, uno de magnesio y uno de zinc.[73]
Esta enzima media la reacción final en la cadena de transporte de electrones y los transfiere al oxígeno, mientras bombea protones a través de la membrana.[74] El aceptor de electrones final es el oxígeno, llamado también aceptor terminal de electrones, el cual es reducido a agua en este paso. Tanto el bombeo directo de protones y la consumición de protones de la matriz en la reducción de oxígeno contribuyen al gradiente de protones. La reacción catalizada es la oxidación de citocromo c y la reducción de oxígeno:
Organización de complejos
editarEl modelo original sobre como los complejos de la cadena respiratoria están organizados era que estos difundían libremente en la membrana mitocondrial.[75] Sin embargo, datos recientes sugieren que los complejos podrían formar estructuras de alto orden llamadas supercomplejos o "respirasomas."[76] En este modelo varios complejos existen como conjuntos organizados de enzimas que interaccionan entre ellas.[77] Estas asociaciones podrían permitir la canalización de sustratos entre varios complejos de enzimas, aumentando su tasa y eficiencia en la transferencia de electrones.[78] Dentro de los supercomplejos presentes en mamíferos, algunos componentes están presentes en mayor cantidad que otros, con una tasa entre complejos I/II/III/IV y ATP sintasa de aproximadamente 1:1:3:7:4.[79] Sin embargo, el debate sobre la hipótesis de estos supercomplejos aún no está resuelta, ya que algunos datos no parecen ajustarse a este modelo.[41][80]
Cadena de transporte de electrones en procariotas
editarEn contraste con la similitud general en cuanto a estructura y función de la cadena de transporte de electrones en eucariotas, las bacterias y arqueas poseen una gran variedad de enzimas de transferencia de electrones. Estas utilizan un conjunto igualmente amplio de sustratos.[81] Al igual que en los eucariotas, la cadena de transporte de electrones de los procariotas utiliza la energía liberada de la oxidación de un sustrato para bombear iones a través de la membrana y generar un gradiente electroquímico. En bacterias, la fosforilación oxidativa en Escherichia coli ha sido estudiada en profundidad, mientras que los sistemas de arqueas han sido poco estudiados.[82]
La principal diferencia entre la fosforilación oxidativa en procariotas y eucariotas es que tanto bacterias como arqueas utilizan una gran variedad de donantes y aceptores de electrones. Esto permite a los procariotas desarrollarse en una amplia variedad de condiciones ambientales.[83] En E. coli, por ejemplo, la fosforilación oxidativa puede ser llevada a cabo por un gran número de pares de agentes reductores y oxidantes, los cuales son listados a continuación. El potencial medio de un químico mide cuanta energía es liberada cuanto este es oxidado o reducido, teniendo los agentes reductores un potencial negativo y los agentes oxidante un potencial positivo.
| Enzima respiratoria | Par redox | Potencial medio
(Volts) |
|---|---|---|
| Formiato deshidrogenasa | Bicarbonato / Formiato | −0,43 |
| Hidrogenasa | Protón / Hidrógeno | −0,42 |
| NADH deshidrogenasa | NAD+ / NADH | −0,32 |
| Glicerol-3-fosfato deshidrogenasa | DHAP / Gli-3-P | −0,19 |
| Piruvato oxidasa | Acetato + Dióxido de carbono / Piruvato | ? |
| Lactato deshidrogenasa | Piruvato / Lactato | −0,19 |
| D-aminoácido deshidrogenasa | 2-oxoácido + Amoníaco / D-aminoácido | ? |
| Glucosa deshidrogenasa | Gluconato / Glucosa | −0,14 |
| Succinato deshidrogenasa | Fumarato / Succinato | +0,03 |
| Ubiquinol oxidasa | Oxígeno / Agua | +0,82 |
| Nitrato reductasa | Nitrato / Nitrito | +0,42 |
| Nitrito reductasa | Nitrito / Amoníaco | +0,36 |
| Dimetil sulfóxido reductasa | DMSO / DMS | +0,16 |
| Trimetilamina N-óxido reductasa | TMAO / TMA | +0,13 |
| Fumarato reductasa | Fumarato / Succinato | +0,03 |
Como se muestra en la tabla anterior, E. coli es capaz de crecer con agentes reductores como el formiato, hidrógeno, o lactato como donantes de electrones, y nitrato, DMSO, u oxígeno como aceptores.[83] La mayor diferencia en el potencial entre un agente oxidante y uno reductor indica una mayor liberación de energía cuando reaccionan. Dentro de estos compuestos, el par succinato/fumarato es inusual, ya que su potencial es muy cercano a cero. El succinato puede ser oxidado a fumarato si se encuentra en presencia de un fuerte agente oxidante como el oxígeno, y el fumarato puede ser reducido utilizando un fuerte agente reductor como lo es el formiato. Estas reacciones alternativas son catalizadas por la succinato deshidrogenasa y la fumarato reductasa, respectivamente.[85]
Algunos procariotas utilizan pares redox que poseen una muy pequeña diferencia de potencial. Por ejemplo, las bacterias nitrificantes tales como Nitrobacter oxidan nitrito a nitrato, donando electrones al oxígeno. La pequeña cantidad de energía liberada en esta reacción es suficiente como para bombear protones y generar ATP, pero no es suficiente como para producir NADH o NADPH directamente para su uso en el anabolismo.[86] Este problema es solucionado utilizando una nitrito oxidorreductasa para producir la suficiente fuerza protón motriz como para hacer funcionar la cadena de transporte de electrones en sentido inverso, haciendo que el complejo I genere NADH.[87][88]
Los procariotas controlan su uso de donantes y aceptores de electrones variando las enzimas que producen, en respuesta a condiciones ambientales.[89] Esta flexibilidad es posible porque diferentes oxidasas y reductasas utilizan las mismas reservas de ubiquinona. Esto permite que muchas combinaciones de enzimas funcionen en conjunto, unidas por un intermediario común de ubiquinol.[84] Por ello es que estas cadenas respiratorias tienen un diseño modular fácilmente intercambiable con otros conjuntos de enzimas.
Además de esta diversidad metabólica, los procariotas también poseen una variedad de isoenzimas – diferentes enzimas que catalizan la misma reacción. Por ejemplo, en E. coli, hay dos tipos diferentes de ubiquinol oxidasa utilizando oxígeno como un aceptor de electrones. Bajo condiciones aeróbicas, la célula utiliza una oxidasa con baja afinidad por el oxígeno que es capaz de transportar dos protones por electrón. Sin embargo, si los niveles de oxígeno caen, cambian a una oxidasa que transfiere solo un protón por electrón, pero tiene una elevada afinidad por el oxígeno.[90]
ATP sintasa (complejo V)
editarATP sintasa, también llamada complejo V, es la enzima final del proceso de la fosforilación oxidativa. Esta enzima se encuentra en todas las formas de vida y funciona de la misma manera tanto en procariotas como en eucariotas.[91] Esta enzima usa la energía almacenada en un gradiente de protones a través de la membrana para llevar a cabo la síntesis de ATP desde ADP y fosfato (Pi). Las estimaciones del número de protones necesarios para sintetizar una molécula de ATP oscilan entre tres y cuatro,[92][93] y algunos investigadores sugieren que las células pueden variar esta proporción, para ajustarse a diferentes condiciones.[94]
Esta reacción de fosforilación es un equilibrio, que puede ser cambiado alterando la fuerza protón motriz. En ausencia de una fuerza protón motriz, la reacción de la ATP sintasa se desplazará hacia la izquierda, hidrolizando ATP y bombeando protones fuera de la matriz a través de la membrana. Sin embargo, cuando la fuerza protón motriz es alta, la reacción es forzada a desplazarse en la dirección opuesta; de izquierda a derecha, permitiendo el flujo de protones en el sentido de su gradiente de concentración produciendo ADP desde ATP.[91] Es más, en la cercanamente relacionada proteína H+-ATPasa tipo vacuolar, la misma reacción es usada para acidificar los compartimentos celulares, bombeando protones e hidrolizando ATP.[95]
La ATP sintasa es un complejo masivo de proteínas con forma de hongo. El complejo de enzimas en mamíferos contiene 16 subunidades y posee una masa de aproximadamente 600 kilodaltons.[96] La porción embebida en la membrana es llamada FO y contiene un anillo de subunidades c y el canal de protones. El pedúnculo y la parte superior esférica es llamada F1 y es el sitio donde ocurre la síntesis de ATP. La porción esférica del extremo de F1 contiene seis proteínas de dos tipos diferentes (tres subunidades α y tres subunidades β), mientras que el "pedúnculo" consiste solo en una proteína: la subunidad γ, con un extremo extendiéndose en la esfera de subunidades α y β.[97] Ambas subunidades, α y β se unen a nucleótidos, pero solo la subunidad β cataliza la síntesis de ATP. Alcanzando por la base una porción de F1 e introduciéndose en la membrana se encuentra una larga subunidad en forma de bastón que ancla las subunidades α y β en la base de la enzima.
A medida que los protones atraviesan la membrana a través del canal en la base de la ATP sintasa, FO entra en rotación.[98] Esta rotación puede ser provocada por cambios en la ionización de aminoácidos en el anillo de subunidades c provocando interacciones electrostáticas que impulsan el anillo de subunidades c a través del canal de protones.[99] Este anillo de rotación provoca la rotación del eje central (el pedúnculo de la subunidad γ) dentro de las subunidades α y β. Estas subunidades son incapaces de rotar debido al brazo lateral que actúa como un estátor. Este movimiento del extremo de la subunidad γ en el interior de la esfera de subunidades α y β provee de energía para los sitios activos en las subunidades β para llevar a cabo un ciclo de movimientos que generan y luego liberan ATP.[100]
La reacción de síntesis de ATP es llamada «mecanismo de cambio de unión» —del inglés binding change mechanism— e involucra el sitio activo de una subunidad β en ciclando a través de tres estados.[11] En el estado "abierto", el ADP y el fosfato entran en el sitio activo (mostrado en marrón en el diagrama). La proteína luego captura las moléculas y se une a ellas ligeramente (mostrado en rojo). La enzima luego cambia su conformación nuevamente y acerca las moléculas, con el sitio activo en el estado final (mostrado en rosado) uniendo el recién formada molécula de ATP con una elevada afinidad. Finalmente, el sitio activo cicla de nuevo a su estado original abierto, liberando ATP y uniéndose a más ADP y fosfato, preparándose así para el próximo ciclo.
En algunas bacterias y arqueas, la síntesis de ATP es llevada a cabo por el movimiento de iones sodio a través de la membrana celular, en lugar del movimiento de protones.[101][102] Arqueas tales como Methanococcus poseen la sintasa A1Ao, una forma de la enzima que contiene proteínas adicionales con muy poca similitud en cuanto a su secuencia con otras subunidades de ATP sintasa de bacterias o eucariotas. Es posible que en algunas especies, la forma A1Ao de la enzima sea una ATP sintasa especializada en el transporte de sodio,[103] pero esto puede que no sea así en todos los casos.[102]
Inhibidores
editarExisten varias drogas y toxinas que inhiben la fosforilación oxidativa. Aunque estas toxinas inhiben solo una enzima en la cadena de transporte de electrones, la inhibición de cualquier paso detiene el resto del proceso. Por ejemplo, cuando la oligomicina inhibe a la enzima ATP sintasa, los protones no pueden ser devueltos a la mitocondria.[104] Como resultado, las bombas de protones son incapaces de operar, y el gradiente se torna demasiado fuerte como para ser superado. NADH deja de ser oxidado y el ciclo del ácido cítrico deja de operar porque la concentración de NAD+ cae por debajo de la concentración que estas enzimas pueden utilizar.
- Cianuro: El cianuro es un potente veneno que inhibe la cadena de transporte de electrones y la fosforilación oxidativa bloqueando el paso de electrones del citocromo a3 al oxígeno en el complejo IV. Esto bloquea la cadena de transporte de electrones, lo que conlleva que no se genere el gradiente de protones y por tanto no se produzca la obtención de ATP con la consiguiente acumulación de NADH y FADH2. Además el cianuro se une a la hemoglobina impidiendo también la captación de oxígeno.
- Oligomicina: La oligomicina, un antibiótico producido por Streptomyces, inhibe a la ATP pasa al unirse a la subunidad Fo e interferir en el transporte de H+ a través de Fo, inhibe por lo tanto la síntesis de ATP y como consecuencia de no eliminar el gradiente de protones se inhibe también a la cadena de transporte de electrones, por lo tanto disminuirá el consumo de O2 y se acumulará NADH y FADH2.
- 2,4-Dinitrofenol: El 2,4-dinitrofenol es un agente desacoplante, es decir, desacopla la cadena de transporte de electrones de la fosforilación oxidativa. El desacoplamiento se produce ya que el 2,4-dinitrofenol hace permeable a los protones de la membrana interna mitocondrial deshaciendo la relación obligada entre la cadena respiratoria y la fosforilación oxidativa. El efecto de este veneno por tanto es la inhibición de la producción de ATP al no generarse el gradiente de pH pero si permite que la cadena de transporte de electrones continúe funcionando.
| Compuesto | Uso | Efecto en la fosforilación oxidativa |
|---|---|---|
| Cianuro y monóxido de carbono |
Veneno | Inhiben la cadena de transporte de electrones ya que se unen más fuertemente que el oxígeno a los centros Fe–Cu en la citocromo c oxidasa, y por tanto evitan la reducción del oxígeno.[105] |
| Oligomicina | Antibiótico | Inhibe la ATP sintasa bloqueando el flujo de protones a través de la subunidad Fo.[104] |
| CCCP 2,4-Dinitrofenol |
Veneno | Ionóforos que interrumpen el gradiente de protones transportando estos a través de la membrana. Este ionoforo desacopla el bombeo de electrones de la ATP sintasa debido a que transporta electrones a través de la membrana mitocondrial interna.[106] |
| Rotenona | Pesticida | Impide la transferencia de electrones del complejo I a la ubiquinona al bloquear los sitios de unión a la ubiquinona.[107] |
| Malonato y oxaloacetato | Inhibidores competitivos de la succinato de hidrogenasa (complejo II).[108] |
No todos los inhibidores de la fosforilación oxidativa son toxinas. En el tejido adiposo marrón, los canales de protones regulados llamados proteínas desacopladoras son capaces de desacoplar la respiración de la síntesis de ATP.[109] Esta respiración rápida produce calor, y es particularmente importante como una vía para mantener la temperatura corporal en la hibernación de los animales, aunque estas proteínas pueden también tener una función más general en la respuesta de las células al estrés oxidativo.[110]
Véase también
editarReferencias
editar- ↑ Chen, Jin-Qiang; Patrick R. Cammarata, Christopher P. Baines, James D. Yager (2009). «Regulation of mitochondrial respiratory chain biogenesis by estrogens/estrogen receptors and physiological, pathological and pharmacological implications». Biochimica et Biophysica Acta (BBA) - Molecular Cell Research 1793 (10): 1540-1570. ISSN 0167-4889. doi:10.1016/j.bbamcr.2009.06.001.
- ↑ Harden, A., Young, W. J. (1906). «The alcoholic ferment of yeast-juice». Proc. R. Soc. (Lond.). B (77): 405-20.
- ↑ Kalckar, H. M. (1974). «Origins of the concept oxidative phosphorylation». Mol. Cell. Biochem. 5 (1-2): 55-63. PMID 4279328. doi:10.1007/BF01874172.
- ↑ Lipmann F, (1941). «Metabolic generation and utilization of phosphate bond energy». Adv Enzymol 1: 99-162.
- ↑ Friedkin, M., Lehninger, A. L. (1 de abril de 1949). «Esterification of inorganic phosphate coupled to electron transport between dihydrodiphosphopyridine nucleotide and oxygen». J. Biol. Chem. 178 (2): 611-23.
- ↑ Slater, E. C. (1953). «Mechanism of Phosphorylation in the Respiratory Chain». Nature 172 (4387): 975. doi:10.1038/172975a0.
- ↑ Mitchell, P. (1961). «Coupling of Phosphorylation to Electron and Hydrogen Transfer by a Chemi-Osmotic type of Mechanism». Nature 191 (4784): 144. PMID 13771349. doi:10.1038/191144a0.
- ↑ Saier Jr, Milton H. «Peter Mitchell and the Vital Force». Archivado desde el original el 30 de agosto de 2006.
- ↑ Mitchell, Peter (1978). «David Keilin's Respiratory Chain Concept and Its Chemiosmotic Consequences» (PDF). Nobel lecture. Nobel Foundation.
- ↑ Pullman, M. E., Penefsky, H. S., Datta, A. y Racker, E. (1 de noviembre de 1960). «Partial Resolution of the Enzymes Catalyzing Oxidative Phosphorylation. I. Purification and Properties of Soluble, Dinitrophenol-stimulated Adenosine Triphosphatase». J. Biol. Chem. 235 (11): 3322-9.
- ↑ a b Gresser, M. J., Myers, J. A., Boyer, P. D. (25 de octubre de 1982). «Catalytic site cooperativity of beef heart mitochondrial F1 adenosine triphosphatase. Correlations of initial velocity, bound intermediate, and oxygen exchange measurements with an alternating three-site model». J. Biol. Chem. 257 (20): 12030-8. PMID 6214554. Archivado desde el original el 29 de septiembre de 2007. Consultado el 7 de agosto de 2009.
- ↑ Boyer, P. D., Cross, R. L., Momsen, W. (1973). «A new concept for energy coupling in oxidative phosphorylation based on a molecular explanation of the oxygen exchange reactions». Proc. Natl. Acad. Sci. U.S.A. 70 (10): 2837-9. PMC 427120. PMID 4517936. doi:10.1073/pnas.70.10.2837.
- ↑ «The Nobel Prize in Chemistry 1997». Nobel Foundation.
- ↑ Sáez, Francisco A.; E. M. F. De Robertis (1977). Biología celular (9na edición). Librería "El Ateneo" Editorial, digitalizado por la Universidad de Texas.
- ↑ Mitchell, P., Moyle, J. (1967). «Chemiosmotic hypothesis of oxidative phosphorylation». Nature 213 (5072): 137-9. PMID 4291593. doi:10.1038/213137a0.
- ↑ Dimroth, P., Kaim, G., Matthey, U. (1 de enero de 2000). «Crucial role of the membrane potential for ATP synthesis by F(1)F(o) ATP synthases». J. Exp. Biol. 203 (Pt 1): 51-9. PMID 10600673.
- ↑ a b c d Schultz, B., Chan, S. (2001). «Structures and proton-pumping strategies of mitochondrial respiratory enzymes». Annu Rev Biophys Biomol Struct 30: 23-65. PMID 11340051. doi:10.1146/annurev.biophys.30.1.23.
- ↑ Rich, P. R. (2003). «The molecular machinery of Keilin's respiratory chain». Biochem. Soc. Trans. 31 (Pt 6): 1095-105. PMID 14641005. doi:10.1042/BST0311095.
- ↑ Porter, R. K., Brand, M. D. (1995). «Mitochondrial proton conductance and H+/O ratio are independent of electron transport rate in isolated hepatocytes». Biochem. J. 310 ((Pt 2)): 379-82. PMC 1135905. PMID 7654171.
- ↑ Mathews, F. S. (1985). «The structure, function and evolution of cytochromes». Prog. Biophys. Mol. Biol. 45 (1): 1-56. PMID 3881803. doi:10.1016/0079-6107(85)90004-5.
- ↑ Wood, P. M. (1983). «Why do c-type cytochromes exist?». FEBS Lett. 164 (2): 223-6. PMID 6317447. doi:10.1016/0014-5793(83)80289-0.
- ↑ Crane, F. L. (1 de diciembre de 2001). «Biochemical functions of coenzyme Q10». Journal of the American College of Nutrition 20 (6): 591-8. PMID 11771674. Archivado desde el original el 16 de diciembre de 2008.
- ↑ Mitchell, P. (1979). «Keilin's respiratory chain concept and its chemiosmotic consequences». Science 206 (4423): 1148-59. PMID 388618. doi:10.1126/science.388618.
- ↑ Søballe, B., Poole, R. K. (1999). «Microbial ubiquinones: multiple roles in respiration, gene regulation and oxidative stress management» (PDF). Microbiology (Reading, Engl.). 145 (Pt 8): 1817-30. PMID 10463148. Archivado desde el original el 29 de mayo de 2008.
- ↑ Johnson, D., Dean, D., Smith, A., Johnson, M. (2005). «Structure, function, and formation of biological iron-sulfur clusters». Annu Rev Biochem 74: 247-81. PMID 15952888. doi:10.1146/annurev.biochem.74.082803.133518.
- ↑ Page, C. C., Moser, C. C., Chen, X., Dutton, P. L. (1999). «Natural engineering principles of electron tunnelling in biological oxidation-reduction». Nature 402 (6757): 47-52. PMID 10573417. doi:10.1038/46972.
- ↑ Leys D, Scrutton NS (2004). «Electrical circuitry in biology: emerging principles from protein structure». Curr. Opin. Struct. Biol. 14 (6): 642-7. PMID 15582386. doi:10.1016/j.sbi.2004.10.002.
- ↑ Boxma B, de Graaf RM, van der Staay GW, et al. (2005). «An anaerobic mitochondrion that produces hydrogen». Nature 434 (7029): 74-9. PMID 15744302. doi:10.1038/nature03343.
- ↑ Vogel, F.; C. Bornhovd, W. Neupert, A. S. Reichert (2006). «Dynamic subcompartmentalization of the mitochondrial inner membrane». The Journal of Cell Biology 175 (2): 237-247. ISSN 0021-9525. doi:10.1083/jcb.200605138.
- ↑ a b c d e f g h Medical CHEMISTRY Compendium. By Anders Overgaard Pedersen and Henning Nielsen. Aarhus University. 2008
- ↑ Hirst, Judy (15 de enero de 2010). «Towards the molecular mechanism of respiratory complex I». The Biochemical Journal 425 (2): 327-339. ISSN 1470-8728. doi:10.1042/BJ20091382.
- ↑ «Energy transducing redox steps of the Na+-pumping NADH:quinone oxidoreductase from Vibrio cholerae». Proc Natl Acad Sci U S A. 107 (28): 12505-10. 2010. PMID 20616050.
- ↑ Scheffler, Immo (2008). Mitochondria (2nd ed. edición). Hoboken N.J.: Wiley-Liss. ISBN 9780470040737.
- ↑ a b PMID 18316732
- ↑ PMID 20025615
- ↑ a b PMID 16873117
- ↑ a b Efremov, Rouslan G.; Rozbeh Baradaran, Leonid A. Sazanov (27 de mayo de 2010). «The architecture of respiratory complex I». Nature 465 (7297): 441-445. ISSN 1476-4687. doi:10.1038/nature09066.
- ↑ Brand, Martin D. (2010). «The sites and topology of mitochondrial superoxide production». Experimental Gerontology 45 (7-8): 466-472. ISSN 0531-5565. doi:10.1016/j.exger.2010.01.003.
- ↑ a b Koopman, Werner J. H.; Leo G. J. Nijtmans, Cindy E. J. Dieteren, Peggy Roestenberg, Federica Valsecchi, Jan A. M. Smeitink, Peter H. G. M. Willems (15 de junio de 2010). «Mammalian mitochondrial complex I: biogenesis, regulation, and reactive oxygen species generation». Antioxidants & Redox Signaling 12 (12): 1431-1470. ISSN 1557-7716. doi:10.1089/ars.2009.2743.
- ↑ Carroll, Joe; Ian M. Fearnley, J. Mark Skehel, Richard J. Shannon, Judy Hirst, John E. Walker (27 de octubre de 2006). «Bovine complex I is a complex of 45 different subunits». The Journal of Biological Chemistry 281 (43): 32724-32727. ISSN 0021-9258. doi:10.1074/jbc.M607135200.
- ↑ a b Lenaz, G., Fato, R., Genova, M., Bergamini, C., Bianchi, C., Biondi, A. (2006). «Mitochondrial Complex I: structural and functional aspects». Biochim Biophys Acta 1757 (9-10): 1406-20. PMID 16828051. doi:10.1016/j.bbabio.2006.05.007.
- ↑ Sazanov, Leonid A. (6 de marzo de 2007). «Respiratory complex I: mechanistic and structural insights provided by the crystal structure of the hydrophilic domain». Biochemistry 46 (9): 2275-2288. ISSN 0006-2960. doi:10.1021/bi602508x.
- ↑ Clason, T.; T. Ruiz, H. Schägger, G. Peng, V. Zickermann, U. Brandt, H. Michel, M. Radermacher (2010-01). «The structure of eukaryotic and prokaryotic complex I». Journal of Structural Biology 169 (1): 81-88. ISSN 1095-8657. doi:10.1016/j.jsb.2009.08.017.
- ↑ Gabaldón, Toni; Daphne Rainey, Martijn A. Huynen (2005). «Tracing the Evolution of a Large Protein Complex in the Eukaryotes, NADH:Ubiquinone Oxidoreductase (Complex I)». Journal of Molecular Biology 348 (4): 857-870. ISSN 0022-2836. doi:10.1016/j.jmb.2005.02.067.
- ↑ Yip, Chui-Ying; Michael E. Harbour, Kamburapola Jayawardena, Ian M. Fearnley, Leonid A. Sazanov (29 de noviembre de 2010). «Evolution of respiratory complex I: 'supernumerary' subunits are present in the {alpha}-proteobacterial enzyme». The Journal of Biological Chemistry. ISSN 1083-351X. doi:10.1074/jbc.M110.194993.
- ↑ Remacle, Claire; M. Rosario Barbieri, Pierre Cardol, Patrice P. Hamel (2008-08). «Eukaryotic complex I: functional diversity and experimental systems to unravel the assembly process». Molecular Genetics and Genomics: MGG 280 (2): 93-110. ISSN 1617-4615. doi:10.1007/s00438-008-0350-5.
- ↑ a b Mckenzie, Matthew; Michael T. Ryan (2010-07). «Assembly factors of human mitochondrial complex I and their defects in disease». IUBMB Life 62 (7): 497-502. ISSN 1521-6551. doi:10.1002/iub.335.
- ↑ Lenaz, Giorgio; Maria Luisa Genova (2010). «Structure and Organization of Mitochondrial Respiratory Complexes: A New Understanding of an Old Subject». Antioxidants & Redox Signaling 12 (8): 961-1008. ISSN 1523-0864. doi:10.1089/ars.2009.2704.
- ↑ Cecchini, G. (2003). «Function and structure of complex II of the respiratory chain». Annu Rev Biochem 72: 77-109. PMID 14527321. doi:10.1146/annurev.biochem.72.121801.161700.
- ↑ Yankovskaya, V., Horsefield, R., Tornroth, S., Luna-Chavez, C., Miyoshi, H., Leger, C., Byrne, B., Cecchini, G., Iwata, S. (2003) «Architecture of succinate dehydrogenase and reactive oxygen species generation.» Science 299, 700–704.
- ↑ Horsefield, R., Iwata, S., Byrne, B. (2004). «Complex II from a structural perspective». Curr. Protein Pept. Sci. 5 (2): 107-18. PMID 15078221. doi:10.2174/1389203043486847.
- ↑ Kita, K., Hirawake, H., Miyadera, H., Amino, H., Takeo, S. (2002). «Role of complex II in anaerobic respiration of the parasite mitochondria from Ascaris suum and Plasmodium falciparum». Biochim. Biophys. Acta 1553 (1-2): 123-39. PMID 11803022. doi:10.1016/S0005-2728(01)00237-7.
- ↑ Painter, H. J., Morrisey, J. M., Mather, M. W., Vaidya, A. B. (2007). «Specific role of mitochondrial electron transport in blood-stage Plasmodium falciparum». Nature 446 (7131): 88-91. PMID 17330044. doi:10.1038/nature05572.
- ↑ Ramsay, R. R., Steenkamp, D. J., Husain, M. (1987). «Reactions of electron-transfer flavoprotein and electron-transfer flavoprotein: ubiquinone oxidoreductase». Biochem. J. 241 (3): 883-92. PMID 3593226.
- ↑ Zhang, J., Frerman, F. E., Kim, J. J. (2006). «Structure of electron transfer flavoprotein-ubiquinone oxidoreductase and electron transfer to the mitochondrial ubiquinone pool». Proc. Natl. Acad. Sci. U.S.A. 103 (44): 16212-7. PMID 17050691. doi:10.1073/pnas.0604567103.
- ↑ Ikeda, Y., Dabrowski, C., Tanaka, K. (25 de enero de 1983). «Separation and properties of five distinct acyl-CoA dehydrogenases from rat liver mitochondria. Identification of a new 2-methyl branched chain acyl-CoA dehydrogenase». J. Biol. Chem. 258 (2): 1066-76. PMID 6401712. Archivado desde el original el 29 de septiembre de 2007. Consultado el 7 de agosto de 2009.
- ↑ Ruzicka FJ, Beinert H (1977). «A new iron-sulfur flavoprotein of the respiratory chain. A component of the fatty acid beta oxidation pathway» (PDF). J. Biol. Chem. 252 (23): 8440-5. PMID 925004. Archivado desde el original el 27 de septiembre de 2007. Consultado el 7 de agosto de 2009.
- ↑ Ishizaki K, Larson TR, Schauer N, Fernie AR, Graham IA, Leaver CJ (2005). «The critical role of Arabidopsis electron-transfer flavoprotein:ubiquinone oxidoreductase during dark-induced starvation». Plant Cell 17 (9): 2587-600. PMC 1197437. PMID 16055629. doi:10.1105/tpc.105.035162.
- ↑ Rasmusson AG, Soole KL, Elthon TE (2004). «Alternative NAD(P)H dehydrogenases of plant mitochondria». Annual review of plant biology 55: 23-39. PMID 15725055. doi:10.1146/annurev.arplant.55.031903.141720.
- ↑ Menz RI, Day DA (1996). «Purification and characterization of a 43-kDa rotenone-insensitive NADH dehydrogenase from plant mitochondria». J. Biol. Chem. 271 (38): 23117-20. PMID 8798503. doi:10.1074/jbc.271.38.23117. Archivado desde el original el 29 de septiembre de 2007. Consultado el 7 de agosto de 2009.
- ↑ McDonald A, Vanlerberghe G (2004). «Branched mitochondrial electron transport in the Animalia: presence of alternative oxidase in several animal phyla». IUBMB Life 56 (6): 333-41. PMID 15370881. doi:10.1080/1521-6540400000876.
- ↑ Sluse FE, Jarmuszkiewicz W (1998). «Alternative oxidase in the branched mitochondrial respiratory network: an overview on structure, function, regulation, and role». Braz. J. Med. Biol. Res. 31 (6): 733-47. PMID 9698817. doi:10.1590/S0100-879X1998000600003.
- ↑ Moore AL, Siedow JN (1991). «The regulation and nature of the cyanide-resistant alternative oxidase of plant mitochondria». Biochim. Biophys. Acta 1059 (2): 121-40. PMID 1883834. doi:10.1016/S0005-2728(05)80197-5.
- ↑ Vanlerberghe GC, McIntosh L (1997). «Alternative oxidase: From Gene to Function». Annual Review of Plant Physiology and Plant Molecular Biology 48: 703-34. PMID 15012279. doi:10.1146/annurev.arplant.48.1.703.
- ↑ Ito Y, Saisho D, Nakazono M, Tsutsumi N, Hirai A (1997). «Transcript levels of tandem-arranged alternative oxidase genes in rice are increased by low temperature». Gene 203 (2): 121-9. PMID 9426242. doi:10.1016/S0378-1119(97)00502-7.
- ↑ Maxwell DP, Wang Y, McIntosh L (1999). «The alternative oxidase lowers mitochondrial reactive oxygen production in plant cells». Proc. Natl. Acad. Sci. U.S.A. 96 (14): 8271-6. PMID 10393984. doi:10.1073/pnas.96.14.8271.
- ↑ Berry E, Guergova-Kuras M, Huang L, Crofts A (2000). «Structure and function of cytochrome bc complexes». Annu Rev Biochem 69: 1005-75. PMID 10966481. doi:10.1146/annurev.biochem.69.1.1005.
- ↑ Crofts AR (2004). «The cytochrome bc1 complex: function in the context of structure». Annu. Rev. Physiol. 66: 689-733. PMID 14977419. doi:10.1146/annurev.physiol.66.032102.150251.
- ↑ Iwata S, Lee JW, Okada K, et al. (1998). «Complete structure of the 11-subunit bovine mitochondrial cytochrome bc1 complex». Science 281 (5373): 64-71. PMID 9651245. doi:10.1126/science.281.5373.64.
- ↑ Trumpower BL (1990). «The protonmotive Q cycle. Energy transduction by coupling of proton translocation to electron transfer by the cytochrome bc1 complex» (PDF). J. Biol. Chem. 265 (20): 11409-12. PMID 2164001. Archivado desde el original el 27 de septiembre de 2007. Consultado el 7 de agosto de 2009.
- ↑ Hunte C, Palsdottir H, Trumpower BL (2003). «Protonmotive pathways and mechanisms in the cytochrome bc1 complex». FEBS Lett. 545 (1): 39-46. PMID 12788490. doi:10.1016/S0014-5793(03)00391-0.
- ↑ Calhoun M, Thomas J, Gennis R (1994). «The cytochrome oxidase superfamily of redox-driven proton pumps». Trends Biochem Sci 19 (8): 325-30. PMID 7940677. doi:10.1016/0968-0004(94)90071-X.
- ↑ Tsukihara T, Aoyama H, Yamashita E, Tomizaki T, Yamaguchi H, Shinzawa-Itoh K, Nakashima R, Yaono R, Yoshikawa S. (1996). «The whole structure of the 13-subunit oxidized cytochrome c oxidase at 2.8 A». Science 272 (5265): 1136-44. PMID 8638158. doi:10.1126/science.272.5265.1136.
- ↑ Yoshikawa S, Muramoto K, Shinzawa-Itoh K, et al. (2006). «Proton pumping mechanism of bovine heart cytochrome c oxidase». Biochim. Biophys. Acta 1757 (9-10): 1110-6. PMID 16904626. doi:10.1016/j.bbabio.2006.06.004.
- ↑ Lenaz, G. (2001). «A critical appraisal of the mitochondrial coenzyme Q pool». FEBS Lett. 509 (2): 151-5. PMID 11741580. doi:10.1016/S0014-5793(01)03172-6.
- ↑ Heinemeyer, J., Braun, H. P., Boekema, E. J., Kouril, R. (2007). «A structural model of the cytochrome C reductase/oxidase supercomplex from yeast mitochondria». J. Biol. Chem. 282 (16): 12240-8. PMID 17322303. doi:10.1074/jbc.M610545200.
- ↑ Schägger, H., Pfeiffer, K. (2000). «Supercomplexes in the respiratory chains of yeast and mammalian mitochondria». EMBO J. 19 (8): 1777-83. PMC 302020. PMID 10775262. doi:10.1093/emboj/19.8.1777.
- ↑ Schägger H (2002). «Respiratory chain supercomplexes of mitochondria and bacteria». Biochim. Biophys. Acta 1555 (1-3): 154-9. PMID 12206908. doi:10.1016/S0005-2728(02)00271-2.
- ↑ Schägger H, Pfeiffer K (2001). «The ratio of oxidative phosphorylation complexes I-V in bovine heart mitochondria and the composition of respiratory chain supercomplexes». J. Biol. Chem. 276 (41): 37861-7. PMID 11483615. doi:10.1074/jbc.M106474200.
- ↑ Gupte S, Wu ES, Hoechli L, et al. (1984). «Relationship between lateral diffusion, collision frequency, and electron transfer of mitochondrial inner membrane oxidation-reduction components». Proc. Natl. Acad. Sci. U.S.A. 81 (9): 2606-10. PMC 345118. PMID 6326133. doi:10.1073/pnas.81.9.2606.
- ↑ Nealson KH (1999). «Post-Viking microbiology: new approaches, new data, new insights». Origins of life and evolution of the biosphere: the journal of the International Society for the Study of the Origin of Life 29 (1): 73-93. PMID 11536899. doi:10.1023/A:1006515817767.
- ↑ Schäfer, G., Engelhard, M., Müller, V. (1999). «Bioenergetics of the Archaea». Microbiol. Mol. Biol. Rev. 63 (3): 570-620. PMC 103747. PMID 10477309.
- ↑ a b Ingledew, W. J., Poole, R. K. (1984). «The respiratory chains of Escherichia coli». Microbiol. Rev. 48 (3): 222-71. PMID 6387427.
- ↑ a b Unden G, Bongaerts J (1997). «Alternative respiratory pathways of Escherichia coli: energetics and transcriptional regulation in response to electron acceptors». Biochim. Biophys. Acta 1320 (3): 217-34. PMID 9230919. doi:10.1016/S0005-2728(97)00034-0.
- ↑ Cecchini G, Schröder I, Gunsalus RP, Maklashina E (2002). «Succinate dehydrogenase and fumarate reductase from Escherichia coli». Biochim. Biophys. Acta 1553 (1-2): 140-57. PMID 11803023. doi:10.1016/S0005-2728(01)00238-9.
- ↑ Freitag A, Bock E (1990). «Energy conservation in Nitrobacter». FEMS Microbiology Letters 66 (1-3): 157-62. doi:10.1111/j.1574-6968.1990.tb03989.x.
- ↑ Starkenburg SR, Chain PS, Sayavedra-Soto LA, et al. (2006). «Genome sequence of the chemolithoautotrophic nitrite-oxidizing bacterium Nitrobacter winogradskyi Nb-255». Appl. Environ. Microbiol. 72 (3): 2050-63. PMID 16517654. doi:10.1128/AEM.72.3.2050-2063.2006.
- ↑ Yamanaka T, Fukumori Y (1988). «The nitrite oxidizing system of Nitrobacter winogradskyi». FEMS Microbiol. Rev. 4 (4): 259-70. PMID 2856189.
- ↑ Iuchi S, Lin EC (1993). «Adaptation of Escherichia coli to redox environments by gene expression». Mol. Microbiol. 9 (1): 9-15. PMID 8412675. doi:10.1111/j.1365-2958.1993.tb01664.x.
- ↑ Calhoun MW, Oden KL, Gennis RB, de Mattos MJ, Neijssel OM (1993). «Energetic efficiency of Escherichia coli: effects of mutations in components of the aerobic respiratory chain» (PDF). J. Bacteriol. 175 (10): 3020-5. PMID 8491720.
- ↑ a b Boyer, P. D. (1997). «The ATP synthase—a splendid molecular machine». Annu. Rev. Biochem. 66: 717-49. PMID 9242922. doi:10.1146/annurev.biochem.66.1.717.
- ↑ Van Walraven HS, Strotmann H, Schwarz O, Rumberg B (1996). «The H+/ATP coupling ratio of the ATP synthase from thiol-modulated chloroplasts and two cyanobacterial strains is four». FEBS Lett. 379 (3): 309-13. PMID 8603713. doi:10.1016/0014-5793(95)01536-1.
- ↑ Yoshida M, Muneyuki E, Hisabori T (2001). «ATP synthase—a marvellous rotary engine of the cell». Nat. Rev. Mol. Cell Biol. 2 (9): 669-77. PMID 11533724. doi:10.1038/35089509.
- ↑ Schemidt RA, Qu J, Williams JR, Brusilow WS (1998). «Effects of carbon source on expression of F0 genes and on the stoichiometry of the c subunit in the F1F0 ATPase of Escherichia coli». J. Bacteriol. 180 (12): 3205-8. PMC 107823. PMID 9620972.
- ↑ Nelson N, Perzov N, Cohen A, Hagai K, Padler V, Nelson H (1 de enero de 2000). «The cellular biology of proton-motive force generation by V-ATPases». J. Exp. Biol. 203 (Pt 1): 89-95. PMID 10600677.
- ↑ Rubinstein JL, Walker JE, Henderson R (2003). «Structure of the mitochondrial ATP synthase by electron cryomicroscopy». Embo J. 22 (23): 6182-92. PMC 291849. PMID 14633978. doi:10.1093/emboj/cdg608.
- ↑ Leslie AG, Walker JE (2000). «Structural model of F1-ATPase and the implications for rotary catalysis». Philos. Trans. R. Soc. Lond., B, Biol. Sci. 355 (1396): 465-71. PMC 1692760. PMID 10836500. doi:10.1098/rstb.2000.0588.
- ↑ Noji H, Yoshida M (2001). «The rotary machine in the cell, ATP synthase». J. Biol. Chem. 276 (3): 1665-8. PMID 11080505. doi:10.1074/jbc.R000021200.
- ↑ Capaldi R, Aggeler R (2002). «Mechanism of the F(1)F(0)-type ATP synthase, a biological rotary motor». Trends Biochem Sci 27 (3): 154-60. PMID 11893513. doi:10.1016/S0968-0004(01)02051-5.
- ↑ Dimroth, P., von Ballmoos, C., Meier, T. (2006). «Catalytic and mechanical cycles in F-ATP synthases. Fourth in the Cycles Review Series». EMBO Rep 7 (3): 276-82. PMC 1456893. PMID 16607397. doi:10.1038/sj.embor.7400646.
- ↑ Dimroth, P. (1994). «Bacterial sodium ion-coupled energetics». Antonie Van Leeuwenhoek 65 (4): 381-95. PMID 7832594. doi:10.1007/BF00872221.
- ↑ a b Becher, B., Müller, V. (1994). «Delta mu Na+ drives the synthesis of ATP via a delta mu Na(+)-translocating F1F0-ATP synthase in membrane vesicles of the archaeon Methanosarcina mazei Gö1». J. Bacteriol. 176 (9): 2543-50. PMC 205391. PMID 8169202.
- ↑ Müller, V. (2004). «An exceptional variability in the motor of archaeal A1A0 ATPases: from multimeric to monomeric rotors comprising 6-13 ion binding sites». J. Bioenerg. Biomembr. 36 (1): 115-25. PMID 15168615. doi:10.1023/B:JOBB.0000019603.68282.04.
- ↑ a b Joshi, S., Huang, Y. G. (1991). «ATP synthase complex from bovine heart mitochondria: the oligomycin sensitivity conferring protein is essential for dicyclohexyl carbodiimide-sensitive ATPase». Biochim. Biophys. Acta 1067 (2): 255-8. PMID 1831660. doi:10.1016/0005-2736(91)90051-9.
- ↑ Tsubaki, M. (1993). «Fourier-transform infrared study of cyanide binding to the Fea3-CuB binuclear site of bovine heart cytochrome c oxidase: implication of the redox-linked conformational change at the binuclear site». Biochemistry 32 (1): 164-73. PMID 8380331. doi:10.1021/bi00052a022.
- ↑ Heytler, P. G. (1979). «Uncouplers of oxidative phosphorylation». Meth. Enzymol. 55: 462-42. PMID 156853. doi:10.1016/0076-6879(79)55060-5.
- ↑ Lambert AJ, Brand MD (2004). «Inhibitors of the quinone-binding site allow rapid superoxide production from mitochondrial NADH: ubiquinone oxidoreductase (complex I)». J. Biol. Chem. 279 (38): 39414-20. PMID 15262965. doi:10.1074/jbc.M406576200.
- ↑ Dervartanian DV, Veeger C. (noviembre de 1964). «Studies on succinate dehydrogenase. I. Spectral properties of the purified enzyme and formation of enzyme-competitive inhibitor complexes». Biochim. Biophys. Acta 92: 233-47. PMID 14249115.
- ↑ Ricquier D, Bouillaud F (2000). «The uncoupling protein homologues: UCP1, UCP2, UCP3, StUCP and AtUCP». Biochem. J. 345 Pt 2: 161-79. PMC 1220743. PMID 10620491. doi:10.1042/0264-6021:3450161.
- ↑ Borecký J, Vercesi AE (2005). «Plant uncoupling mitochondrial protein and alternative oxidase: energy metabolism and stress». Biosci. Rep. 25 (3-4): 271-86. PMID 16283557. doi:10.1007/s10540-005-2889-2.
Lecturas complementarias
editarIntroductorias
- Nelson DL; Cox MM (2007). Lehninger Principios de Bioquímica (5ta edición). Omega, S.A., Barcelona. ISBN 9788428214865.
- Schneider ED; Sagan D (2006). Into the Cool: Energy Flow, Thermodynamics and Life (1ª edición). University of Chicago Press. ISBN 0-226-73937-6.
- Lane N (2006). Power, Sex, Suicide: Mitochondria and the Meaning of Life (1ª edición). Oxford University Press, EE. UU. ISBN 0199205647.
Avanzadas
- Nicholls DG; Ferguson SJ (2002). Bioenergetics 3 (1ª edición). Academic Press. ISBN 0-125-18121-3.
- Haynie D (2001). Biological Thermodynamics (1ª edición). Cambridge University Press. ISBN 0-521-79549-4.
- Rajan SS (2003). Introduction to Bioenergetics (1ª edición). Anmol. ISBN 8-126-11364-2.
- Wikstrom M (Ed) (2005). Biophysical and Structural Aspects of Bioenergetics (1ª edición). Royal Society of Chemistry. ISBN 0-854-04346-2.
Enlaces externos
editar- Diagramas animados ilustrando la fosforilación oxidativa. Wiley and Co Concepts in Biochemistry (en inglés).
- Fosforilación oxidativa. Metabolic Pathways of Biochemistry, de la Universidad George Washington (en inglés).
- Lecturas de biofísica Archivado el 2 de mayo de 2009 en Wayback Machine. de Antony Crofts, Universidad de Illinois en Urbana-Champaign (en inglés).
- Esta obra contiene una traducción derivada de «Oxidative phosphorylation» de Wikipedia en inglés, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.