Diclofenaco
El diclofenaco es un fármaco inhibidor relativamente no selectivo de la ciclooxigenasa y miembro de la familia de los antiinflamatorios no esteroideos (AINE). Está indicado para reducir inflamaciones y como analgésico. Se puede usar para reducir los cólicos menstruales.
| Diclofenaco | ||
|---|---|---|
 | ||
| Nombre (IUPAC) sistemático | ||
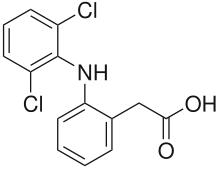
| Ácido 2-(2-[(2,6-diclorofenyl)amino]fenil)acético | ||
| Identificadores | ||
| Número CAS | 15307-86-5 | |
| Código ATC | M01AB05 D11AX18; M02AA15; S01BC03 | |
| PubChem | 3033 | |
| DrugBank | DB00586 | |
| Datos químicos | ||
| Fórmula | C14H11NCl2O2 | |
| Peso mol. | 296.148 g/mol | |
| Farmacocinética | ||
| Biodisponibilidad | 100 % | |
| Metabolismo | hepático, no tiene metabolitos activos | |
| Excreción |
Diclofenaco inalterado: biliar, únicamente 1 % en la orina Metabolitos: 35 % biliar, 65 % en orina | |
| Datos clínicos | ||
| Nombre comercial |
Voltaren Voltadol Forte | |
| Cat. embarazo | A (AU) B (1.º y 2.º trimestres), X (3.er trimestre).[1] | |
| Estado legal | POM (UK) La mayor parte de sus preparaciones se venden con receta; solo en varios países se vende sin receta. Fabricación y uso veterinario prohibido en India, Nepal, Pakistán debido a la inminente extinción de los buitres locales. | |
| Vías de adm. | Oral, rectal, intramuscular, intravenoso (renal y cálculos), tópico | |
El diclofenaco es un derivado fenilacético.[2]
Mecanismo de acción
editarEl mecanismo de acción consiste en evitar la síntesis de prostaglandinas mediante la inhibición de la enzima ciclooxigenasa (COX).
La inhibición del COX-1 también disminuye la producción de prostaglandinas en el epitelio del estómago, haciéndolo mucho más vulnerable a la corrosión por los ácidos gástricos., por lo que este es el principal efecto secundario del diclofenaco.
El diclofenaco posee una preferencia baja a moderada (aproximadamente unas diez veces) a bloquear el isoenzima COX2, y se cree que por eso posee una baja incidencia de efectos negativos gastrointestinales, en comparación con los mostrados por la indometacina y el ácido acetilsalicílico.
Existen evidencias de que el diclofenaco inhibe las funciones de la lipooxigenasa,[3] por lo que reduce la formación de leucotrienos (sustancias inflamatorias). También se especula que el diclofenaco inhibe la producción de la enzima fosfolipasa A2 en su mecanismo de acción. Estas acciones adicionales explican su alta efectividad.[4]
Hay marcadas diferencias entre los antiinflamatorios no esteroideos en su inhibición selectiva de los dos subtipos de ciclooxigenasa, COX-1 y COX-2. Muchos medicamentos han sido diseñados para centrarse en la inhibición de COX-2 como una forma de minimizar los efectos gastrointestinales de otros antiinflamatorios no esteroideos como el ácido acetilsalicílico. En la práctica, el uso de algunos inhibidores de COX-2, como el meloxicam ha traído como consecuencia numerosos paros cardiacos de pacientes que no resistieron el tratamiento; sin embargo, en otro grupo significativo de pacientes que usaron inhibidores de COX, como el diclofenaco, ha sido perfectamente tolerado.[5]
Excreción
editarEl diclofenaco experimenta metabolismo hepático y luego excreción urinaria y biliar de los metabolitos conjugados. Poco o nada de diclofenaco inalterado es excretado en la orina. Aproximadamente 65 % de la dosis es excretada en la orina y 35 % en la bilis. Debido a que los metabolitos no son activos ya que el riñón no es una vía importante para la eliminación de diclofenaco inalterado, no es necesario realizar un ajuste de dosis en pacientes con insuficiencia renal leve a moderada. La vida media de eliminación es de aproximadamente 2 horas.[6]
Indicaciones
editarEn padecimientos musculoesqueléticos, en especial artritis (artritis reumatoide, osteoartritis, espondiloartritis, espondilitis anquilosante), ataques de gota y manejo del dolor causado por cálculos renales y vesiculares. El diclofenaco se usa regularmente para tratar el dolor leve a moderado posterior a cirugía o tras un proceso traumático, particularmente cuando hay inflamación presente. El fármaco es efectivo contra el dolor menstrual. En supositorios rectales, el diclofenaco puede considerarse el medicamento de primera elección para la analgesia preventiva y la náusea posoperatoria.[2]
El uso de diclofenaco a largo plazo, al igual que con otros AINEs, predispone a la aparición de úlceras pépticas, por lo que muchos pacientes con esta predisposición reciben tratamiento de diclofenaco en combinación con misoprostol, un análogo sintético de las prostaglandinas que protege la mucosa gástrica en un solo producto.[7]
Ha surgido un producto con diclofenaco al 3 % con base de gel para el tratamiento de la queratosis actínica, la cual es un padecimiento causado por una sobreexposición a la luz solar.[8]
Existen también presentaciones con licencia venta sin receta como el diclofenaco al 1 % en emulgel para emplearse contra dolores leves y para tratar padecimientos musculoesqueléticos.[9]
Muchos países venden al público colirios para tratar la inflamación aguda y crónica, no causada por bacterias, en la parte anterior del ojo (por ejemplo, en estados postquirúrgicos), sin embargo no existen evidencias concluyentes de que en verdad funcione.[10]
Usos empíricos
editarEn caso necesario, el diclofenaco se puede combinar con derivados opiáceos. En Europa existen marcas comerciales con una combinación de diclofenaco y codeína a razón de 50mg de cada componente (Combarén®) para el tratamiento del dolor del cáncer.[11]
Se creía que diclofenaco y otros AINEs puede ayudar a proteger contra el desarrollo de la enfermedad de Alzheimer,[12] sin embargo, la evidencia sugiere que no hay efecto beneficioso de los AINEs en la cognición o la gravedad general de la enfermedad. Por lo tanto, aunque se necesita más investigación en el campo, la evidencia disponible no respalda el uso de AINEs para el tratamiento de la enfermedad de Alzheimer.[13]
Se ha visto que el diclofenaco eleva la presión sanguínea en pacientes con el síndrome Shy-Drager (hipotensión autónoma) que a veces se presenta en pacientes con diabetes. Actualmente, esto está en investigación, por lo que no se recomienda como tratamiento de rutina.[14]
El diclofenaco tiene la capacidad de tratar los síntomas relacionados con las ITU (infecciones del tracto urinario) no complicadas causadas por la E. coli, ya que puede aliviar el dolor y la inflamación.[15]
La administración posoperatoria de diclofenaco puede tener un papel protector contra el desarrollo del síndrome de pospericardiotomía después de la cirugía cardíaca.[16]
Contraindicaciones
editar- Hipersensibilidad reconocida al diclofenaco
- Historia de reacciones alérgicas (broncoespasmo, choque, rinitis, urticaria) después del uso de ácido acetilsalicílico u otros AINE
- Tercer trimestre del embarazo
- Ulceración estomacal y/o duodenal activa
- Sangrado gastrointestinal
- Padecimientos inflamatorios intestinales tales como enfermedad de Crohn o colitis ulcerativa
- Insuficiencia cardiaca severa (según la clasificación NYHAIII/IV, de la Asociación Cardiológica de Nueva York).
- Insuficiencia hepática grave (clase C, según la escala Child-Pugh).
- Insuficiencia renal grave (depuración de creatinina < 30 ml/min).
- Hay que tener cuidado en pacientes con porfiria hepática preexistente, ya que el diclofenaco puede disparar los ataques.
- Se debe tener cuidado especial en pacientes con sangrado intenso (como hemorragia cerebral).
- Disfunción eréctil.
- Disminución de la vista.
Efectos secundarios
editar- El 20 % de los pacientes en tratamientos a largo plazo experimentan efectos secundarios y, de éstos, un 2 % tienen que descontinuar el uso del fármaco debido principalmente a efectos gastrointestinales, sangramiento gastrointestinal oculto y ulceración gástrica —aunque las úlceras ocurren con menor frecuencia que el de otros AINE.
- Los problemas que más se ven en la práctica son los gastrointestinales. El desarrollo de ulceraciones o sangrado requiere terminación inmediata de la terapia con diclofenaco. Como profilaxis durante los tratamientos largos, la mayoría de los pacientes pueden recibir algún fármaco protector de la úlcera (por ejemplo, 150 mg de ranitidina o de misoprostol al acostarse, 20 mg de omeprazol al acostarse).
- Poco frecuente es la depresión de la médula ósea (leucopenia, agranulocitosis, trombopenia con o sin púrpura, anemia aplásica). En caso de ser detectadas tardíamente, estos padecimientos pueden ser una amenaza contra la vida y ser de carácter irreversible. Todos los pacientes recibirán vigilancia estricta. El diclofenaco es un inhibidor débil y reversible de la agregación trombocítica, evento requerido para una coagulación sanguínea normal.
- No es frecuente que se presenten daño renal o hepático, aunque suelen ser reversibles. Rara vez puede presentarse hepatitis sin ningún síntoma de advertencia, y podría ser fatal. Los pacientes con osteoartritis desarrollan más frecuentemente síntomas de enfermedad hepática que los pacientes con artritis reumatoide. La función renal y hepática deberán vigilarse con regularidad durante los tratamientos de larga duración.
- Específicamente, se sabe que el diclofenaco provoca falla renal en buitres asiáticos (véase problemas ambientales). Se sabe que algunas especies y algunas personas son sensibles a algunas sustancias adictivas, y se sospecha que no expresan algunos genes faltantes relacionados con enzimas específicas de desintoxicación de dichas sustancias. Dado que los individuos mayores tiene una reducida expresión de todos los niveles de enzimas, el metabolismo de los ancianos podría aproximarse gradualmente al observado en los buitres, lo que los vuelve inesperadamente vulnerables e intolerantes al diclofenaco.
- Los AINE "están asociados con efectos renales adversos causados por la reducción de la síntesis renal de prostaglandinas"[17] en personas o especies animales sensibles, y potencialmente durante el uso por largos periodos en personas no sensibles, la resistencia a los efectos colaterales disminuye con la edad. Desafortunadamente este efecto colateral no puede ser evitado simplemente por el uso de un inhibidor selectivo COX-2 porque, "Ambas isoformas de COX, COX-1 y COX-2, son expresadas en el riñón. Consecuentemente, las mismas precauciones relacionadas al riesgo de daño renal que son observadas para AINE no selectivos, deberán ser observadas también cuando inhibidores selectivos COX-2 sean administrados."[17]
- Posterior a la identificación del riesgo incrementado de ataques cardiacos con el Inhibidor COX-2 rofecoxib en el 2004, la atención se ha enfocado en todos los otros miembros del grupo AINE, incluyendo al diclofenaco. Los resultados de investigación son una mezcla de metaanálisis de artículos y reportes actualizados hasta abril del 2006 que sugieren un rango relativamente incrementado de enfermedad cardiaca de 1,g3, en comparación con los no usuarios.[18] El profesor Peter Weissberg, director médico de la Fundación Británica del Corazón dijo, "Sin embargo, el riesgo incrementado es pequeño y muchos pacientes con dolor crónico debilitante podrían sentir muy bien que este pequeño riesgo vale la pena a fin de aliviar sus síntomas". Solo el naproxeno ha sido hallado como el único que no incrementa el riesgo de enfermedad cardíaca, pero se sabe que el naproxeno tiene un rango mayor de producción de úlcera gástrica que el diclofenaco.
Un amplio estudio subsecuente de 74 838 usuarios de AINE o de los coxibs, publicado en mayo de 2006, no encontró riesgo cardiovascular adicional por el uso de diclofenaco.[19] - En octubre de 2020, la Administración de Drogas y Alimentos de los EE. UU . (FDA) requirió que la etiqueta del medicamento se actualizara para todos los medicamentos antiinflamatorios no esteroides para describir el riesgo de problemas renales en los bebés por nacer que resultan en un nivel bajo de líquido amniótico.[20] Recomiendan evitar los AINE en mujeres embarazadas a las 20 semanas o más tarde del embarazo.[21]
Formas farmacéuticas
editarPresentaciones
editarPor sus propiedades fisicoquímicas y requisitos de conservación, entre los excipientes habituales para este producto nos podemos encontrar con los siguientes:
| Forma farmacéutica | Presentación | Laboratorio | Denominación |
| SOLUCIÓN INYECTABLE INTRAMUSCULAR | CAJA CON 1 AMPOLLA DE VIDRIO TIPO I POR 3 ML CADA UNA | TECNOQUIMICA S S.A | DICLOFENACO SÓDICO |
| SOLUCIÓN INYECTABLE INTRAVENOSA | CAJA X 1 AMPOLLA DE VIDRIO TIPO I INCOLORO X 3 ML C/U | VITALIS S.A.C.I | DICLOFENACO SÓDICO |
| CÁPSULAS DE LIBERACIÓN PROLONGADA | CAJA PLEGADIZA CON 1 BLISTER POR 2, 5 O 10 CÁPSULAS DE LIBERACIÓN PROLONGADA 100 MG | LABORATORIOS MK S.A.S Y LABORATORIOS LA SANTÉ S.A | DICLOFENACO SÓDICO MICROGRANULOS DE LIBERACIÓN PROLONGADA |
| CÁPSULAS DE LIBERACIÓN RETARDADA | CAJA POR 2 CÁPSULAS EN BLISTER PELLETS DE LIBERACIÓN PROLONGADA AL 40% | AMERICAN GENERICS S.A.S. | DICLOFENACO RETARD |
| TABLETA RECUBIERTA | CAJA POR 10 TABLETAS RECUBIERTAS EN 50 MG | MEMPHIS PRODUCTS S.A. | DICLOFENACO SÓDICO |
| TABLETA RECUBIERTA | CAJA X 10 TABLETAS 30/50MG | “DORNAX” | CODEÍNA DICLOFENACO SÓDICO |
| TABLETAS CON O SIN RECUBRIR | CAJA X 10 GRAGEAS EN BLISTER PVC/ALUMINIO 50MG | LABORATORIOS ECAR S.A | DICLOFENACO GRAGEAS |
| TABLETAS CON O SIN RECUBRIR | BLISTER PVC/ ALUMINIO POR 10 TABLETAS POR 50 MG ( 25 MG/25MG) | TECNOQUIMICAS S.A | DICLOFENACO SODICO /TRAMADOL HCL |
| TABLETAS DE LIBERACIÓN RETARDADA | BLISTER PVC/ ALUMINIO POR 10 TABLETAS POR 50 MG | LABORATORIO PROFESIONAL FARMACEUTICO S.A.S. - LABORATORIOS LAPROFF S.A.S | DICLOFENACO SÓDICO |
| GELES | TUBO COLAPSIBLE DE ALUMINIO CON RECUBRIMIENTO INTERNO DE LACA EPOXIFENOLICA, POR 40/50 G. DE GEL. | MEMPHIS PRODUCTS S.A | DICLOFENACO GEL |
| GELES | TUBO COLAPSIBLE DE ALUMINIO POR 50G EN CAJA INDIVIDUAL | GENFAR S.A Y LABORATORIOS RICHMOND COLOMBIA S.A.S. Y COOPIDROGAS Y GSK (VOLTAREN) | DICLOFENACO GEL AL 1% |
| SUPOSITORIO | CADA ESTUCHE CONTIENE 12 SUPOSITORIOS 100MG | LABORATORIO LLORENS | DICLOFENACO LLORENS |
| SOLUCIÓN OFTÁLMICA | SOLUCIÓN OFTÁLMICA X 5ML | LAB. BLASKOV | DICLOFENACO SÓDICO 0,1% |
Tabla realizada con fuentes de INVIMA Colombia[22] y del Centro de información online de medicamentos de la AEMPS - CIMA[23]
Problemas ecológicos
editarSe ha constatado que el uso veterinario del diclofenaco llevó a un decrecimiento importante en la población de buitres en el subcontinente indio, hasta de un 95 % en ciertas áreas.[24][19][25]
El mecanismo de la muerte fue probablemente la insuficiencia renal, un conocido efecto secundario del diclofenaco. Los buitres comen restos humanos y de animales domésticos tratados veterinariamente con diclofenaco, y se envenenan debido al compuesto químico acumulado. Durante la reunión de la National Wildlife Board en marzo de 2005, el gobierno de India anunció que espera terminar con el uso de diclofenaco en animales.[26] El candidato para reemplazar al diclofenaco es el meloxicam, que es más seguro (aunque más caro).[27] Es más caro que el diclofenaco, pero su precio está disminuyendo debido a que más farmacéuticas están empezando a fabricarlo.[28]
Uso en veterinaria
editarA pesar de estas alternativas, el diclofenaco ha sido autorizado para su uso con ganado en Italia y, desde 2013, en España donde habitan el 90 % de los buitres de Europa, y comienza a ser ampliamente accesible en el mercado interior de la Unión Europea. SEO/BirdLife, junto con la federación BirdLife y la VCF llevan a cabo una campaña para evitar el desastre ecológico y económico.[29][30][31] Tan sólo en España, los buitres evitan la emisión de casi 200.000 toneladas al año de gases de efecto invernadero al consumir cadáveres que, de otra forma, serían incinerados.[29]
Referencias y notas
editar- ↑ Drugs. «Diclofenaco en embarazo y lactancia». Consultado el 19 de octubre de 2021.
- ↑ a b Katzung, Bertram G. (2007). «Chapter 36. Nonsteroidal Anti-Inflammatory Drugs, Disease-Modifying Antirheumatic Drugs, Nonopioid Analgesics, & Drugs Used in Gout». Basic & Clinical Pharmacology (9 edición). McGraw-Hill. ISBN 0071451536.
- ↑ Gan, TJ (Julio de 2010). «Diclofenac: an update on its mechanism of action and safety profile.». Current medical research and opinion 26 (7): 1715-31. PMID 20470236.
- ↑ Ebrahimi, M; Firuzi, O; Miri, R; Razzaghi-Asl, N; Ebadi, A (22 de noviembre de 2016). «Structural Insight into Binding Mode of 9-Hydroxy Aristolochic Acid, Diclofenac and Indomethacin to PLA2.». Interdisciplinary sciences, computational life sciences. PMID 27878455.
- ↑ Dalal, D; Dubreuil, M; Peloquin, C; Neogi, T; Zhang, Y; Choi, H; Felson, D (Diciembre de 2017). «Meloxicam and risk of myocardial infarction: a population-based nested case-control study.». Rheumatology international 37 (12): 2071-2078. PMID 29030657.
- ↑ «Diclofenac - FDA prescribing information, side effects and uses». www.drugs.com. Consultado el 22 de mayo de 2016.
- ↑ Morant, SV; Shield, MJ; Davey, PG; MacDonald, TM (2002). «A pharmacoeconomic comparison of misoprostol/diclofenac with diclofenac.». Pharmacoepidemiology and drug safety 11 (5): 393-400. PMID 12271881.
- ↑ Martin, GM; Stockfleth, E (de mayo de 2012). «Diclofenac sodium 3% gel for the management of actinic keratosis: 10+ years of cumulative evidence of efficacy and safety.». Journal of drugs in dermatology : JDD 11 (5): 600-8. PMID 22527428.
- ↑ Tavano, L; Mazzotta, E; Muzzalupo, R (29 de enero de 2018). «Innovative topical formulations from diclofenac sodium used as surfadrug: The birth of Diclosomes.». Colloids and surfaces. B, Biointerfaces 164: 177-184. PMID 29413594.
- ↑ Wakai, A; Lawrenson, JG; Lawrenson, AL; Wang, Y; Brown, MD; Quirke, M; Ghandour, O; McCormick, R; Walsh, CD; Amayem, A; Lang, E; Harrison, N (18 de mayo de 2017). «Topical non-steroidal anti-inflammatory drugs for analgesia in traumatic corneal abrasions.». The Cochrane database of systematic reviews 5: CD009781. PMID 28516471.
- ↑ Strobel, E (10 de agosto de 1992). «[Drug therapy in severe tumor pain. Comparative study of a new combination preparation versus diclofenac-Na].». Fortschritte der Medizin 110 (22): 411-4. PMID 1381330.
- ↑ Nevado-Holgado, AJ; Lovestone, S (2017). «Determining the Molecular Pathways Underlying the Protective Effect of Non-Steroidal Anti-Inflammatory Drugs for Alzheimer's Disease: A Bioinformatics Approach.». Computational and structural biotechnology journal 15: 1-7. PMID 27872687.
- ↑ Miguel-Álvarez, M; Santos-Lozano, A; Sanchis-Gomar, F; Fiuza-Luces, C; Pareja-Galeano, H; Garatachea, N; Lucia, A (Febrero de 2015). «Non-steroidal anti-inflammatory drugs as a treatment for Alzheimer's disease: a systematic review and meta-analysis of treatment effect.». Drugs & aging 32 (2): 139-47. PMID 25644018.
- ↑ Nicolae, Sfetcu (2014). Health & Drugs - Disease, Prescription & Medication (1a edición). LULU Press. ISBN 9781312039995.
- ↑ estudio
- ↑ Sevuk, U; Baysal, E; Altindag, R; Yaylak, B; Adiyaman, MS; Ay, N; Alp, V; Beyazit, U (2015). «Role of diclofenac in the prevention of postpericardiotomy syndrome after cardiac surgery.». Vascular health and risk management 11: 373-8. PMID 26170687.
- ↑ a b Brater DC (2002). «Renal effects of cyclooxygyenase-2-selective inhibitors». J Pain Symptom Manage 23 (4 Suppl): S15-20; discussion S21-3. PMID 11992745.
- ↑ Kearney P, Baigent C, Godwin J, Halls H, Emberson J, Patrono C (2006). «Do selective cyclo-oxygenase-2 inhibitors and traditional non-steroidal anti-inflammatory drugs increase the risk of atherothrombosis? Meta-analysis of randomised trials.». BMJ 332 (7553): 1302-8. PMID 16740558.
- ↑ a b Solomon D, Avorn J, Stürmer T, Glynn R, Mogun H, Schneeweiss S (2006). «Cardiovascular outcomes in new users of coxibs and nonsteroidal antiinflammatory drugs: high-risk subgroups and time course of risk.». Arthritis Rheum 54 (5): 1378-89. PMID 16645966.
- ↑ Research, Center for Drug Evaluation and (27 de octubre de 2020). «FDA recommends avoiding use of NSAIDs in pregnancy at 20 weeks or later because they can result in low amniotic fluid». FDA (en inglés). Consultado el 19 de octubre de 2021.
- ↑ Commissioner, Office of the (16 de octubre de 2020). «FDA Warns that Using a Type of Pain and Fever Medication in Second Half of Pregnancy Could Lead to Complications». FDA (en inglés). Consultado el 19 de octubre de 2021.
- ↑ «Consultas INVIMA».
- ↑ «.:: CIMA ::. Centro de información de medicamentos». cima.aemps.es. Consultado el 18 de julio de 2023.
- ↑ Oaks JL, Gilbert M, Virani MZ, Watson RT, Meteyer CU, Rideout BA, Shivaprasad HL, Ahmed S, Chaudhry MJ, Arshad M, Mahmood S, Ali A, Khan AA (2004). «Diclofenac residues as the cause of vulture population decline in Pakistán». Nature 427 (6975): 630-3. PMID 14745453.
- ↑ El Mundo (8 de julio de 2006). «La India pierde a sus buitres». Consultado el 28 de diciembre de 2007.
- ↑ «Saving the vultures from extiction». Press Information Bureau, Government of India. 16 de mayo de 2005. Consultado el 12 de mayo de 2006.
- ↑ Swan G, Naidoo V, Cuthbert R, Green RE, Pain DJ, Swarup D, Prakash V, Taggart M, Bekker L, Das D, Diekmann J, Diekmann M, Killian E, Meharg A, Patra RC, Saini M, Wolter K (2006). «Removing the threat of diclofenac to critically endangered Asian vultures». PLoS Biol 4 (3): e66. PMC 1351921. PMID 16435886. doi:10.1371/journal.pbio.0040066.
- ↑ Gill, V. New drug threat to Asian vultures (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última). BBC News December 9, 2009.
- ↑ a b «Diclofenaco el fármaco que mató millones de buitres en Asia llega a España».
- ↑ «Vulture killing drug now available on EU market». Archivado desde el original el 24 de abril de 2014. Consultado el 24 de abril de 2014.
- ↑ «Diclofenac in Europe – the battle rages on!».
Enlaces externos
editar- En Epistemoikos hay más información sobre Diclofenaco.