Amalgama (odontología)
La amalgama es un material de restauración utilizado en odontología, con frecuencia se utiliza para restaurar dientes afectados por caries y resulta de la aleación del mercurio con otros metales, como cobre, zinc, plata, estaño u oro y otras clases de metales.
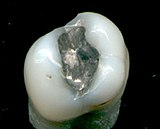
En odontología, se habla más concretamente de "amalgama de plata", para referirse a la aleación utilizada para obturar las cavidades que aparecen como consecuencia de las caries y así restablecer la función masticatoria y devolver estabilidad mediante la reposición con este material de los tejidos perdidos. La amalgama se colocará en alguna de las cavidades de Black según el tipo de lesión que haya que obturar. Estas son siempre retentivas ya que la amalgama no se adhiere al tejido dentario.
Las principales ventajas de la amalgama dental respecto a los empastes de composite son su larga durabilidad y su bajo costo. Sus desventajas son el color plateado, poco estético para los pacientes y la cantidad de tejido dentario que hay que extraer para su uso. También producen un aumento en la exposición a mercurio tanto en quienes las portan[1] como en los odontólogos y sus asistentes.[2] Como consecuencia de la cremación de cadáveres, las amalgamas dentales son causa de una parte importante de las emisiones de mercurio a la atmósfera, y producen residuos contaminantes en el aire, la basura y los desagües de las consultas de odontología.[3] Los residuos inducen envenenamiento por mercurio debido a su bioacumulación.
Su uso está prohibido desde 2008 en Suecia, Noruega y Dinamarca[4] y está restringido en otros países para algunos grupos de población. Se estudia su prohibición en toda la Unión Europea debido al impacto que tienen sobre el medio ambiente.[5]
Preparación
editarLas amalgamas dentales se comercializan en distintas formas. En un formato típico, una amalgama dental se encuentra en una cápsula predosificada que contiene 400 mg de polvo de aleación y 350-420 mg de mercurio metálico. Ambos materiales se encuentran separados en el interior de la cápsula. Cuando esta se presiona entran en contacto, y mediante una máquina llamada amalgamador, que produce una vibración rápida y uniforme, se mezclan. A este proceso se le conoce como amalgamación. El proceso de amalgamación da lugar a la amalgama, un material dúctil que puede ser moldeado en el interior de las cavidades de Black de modo que tome la forma adecuada para su retención.
También es posible realizar esta mezcla de manera manual, como se empezó haciendo en sus orígenes. Siguiendo este procedimiento las cantidades de aleación y de mercurio se toman de manera aproximada y se mezclan manualmente en una cubeta. Esta forma de preparación hace que muy a menudo no se cumplan las especificaciones del fabricante,[6] y que el personal odontológico sufra una mayor exposición a los vapores de mercurio,[7] que a lo largo de años puede ser perjudicial.[8]
Tipos de amalgamas
editarAmalgama de cobre
editarEste tipo de amalgamas no se encuentran reguladas en ningún estándar ISO y no deben confundirse con las amalgamas no gamma II. Están en desuso debido a su alta inestabilidad respecto a otras amalgamas.[9] Su composición era:[10]
Mercurio: 70% Cobre: 30% Cadmio (en ocasiones): < 1,5% (Neo-Silbrin, Cupromuc)
Amalgama convencional (baja en cobre)
editarLas amalgamas convencionales fueron propuestas en 1896 por a G.V. Black.[11] En 1978 la composición de la aleación fue estandarizada en la norma ISO 1559,[12] siendo su composición :
Plata: < 64%. Estaño: < 29%. Cobre: < 6%. Mercurio: < 3%. (Previo a la amalgamación) Zinc: < 2%.
Tras la amalgamación, el porcentaje de mercurio por peso es de un 50% aproximadamente.
Amalgama no gamma II (alta en cobre)
editarEn 1963 los profesores Innes y Youdelis de la universidad de Windsor dieron una nueva fórmula para la aleación de amalgamas dentales. En 1986 se ajustó la norma ISO para incluir esta formulación, dando lugar al ISO 1559 2ª ed,[13] siendo su composición:
Plata: > 40%. Estaño: < 32%. Cobre: < 30%. Mercurio: < 3%. (Previo a la amalgamación) Zinc: < 2%.
Tras la amalgamación, el porcentaje de mercurio por peso es de un 50% aproximadamente.
Posibles riesgos
editarAumento en la exposición al mercurio
editarEn 1991 la Organización Mundial de la Salud determinó que las amalgamas dentales son una fuente significativa de exposición a mercurio para la población general.[14] Una amalgama dental suele contener entre 120 y 570 mg de este elemento.[15] Este mercurio se libera muy lentamente en la cavidad oral en forma de vapores de mercurio y de iones en la saliva. Las medidas intraorales muestran que en circunstancias normales una persona con amalgamas dentales se expone a través de ellas a una dosis de entre 2.4 y 17 µg/día.[1] El mercurio en la orina muestra dosis similares, de entre 4 y 20 µg/día.[16] Sin embargo, se han registrado casos en los que la dosis procedente de amalgamas era de 100 µg/día.[17] Durante su puesta y extracción se producen las dosis más elevadas,[18] por lo que para estas operaciones se ha propuesto el uso de un suministro de aire limpio por vía nasal, dique de goma y succionador de aire para evitar la exposición del paciente, así como máscaras con filtro de mercurio para el odontólogo y su asistente.[19] Algunas personas con síntomas variados y de tipo mental en mayor medida atribuibles a un envenenamiento por mercurio, experimentan mejoría tras las extracción de sus empastes de amalgama.[20][21][22][23][24]
Aspectos toxicológicos
editarLos vapores de mercurio son absorbidos en los pulmones en un 80%, desde donde el mercurio elemental se incorpora a la circulación sanguínea.[25][26] El mercurio en forma elemental Hg0 atraviesa la barrera hematoencefálica, sin embargo una vez es oxidado a su forma divalente Hg2+ ya no puede hacerlo. La semivida de eliminación del mercurio en la sangre suele ser de menos de 90 días, aunque en algunos casos es mayor.[27] La enzima catalasa oxida rápidamente el Hg0 a su forma divalente Hg2+.[28][29] Parte del Hg0 absorbido en los pulmones es oxidado en el interior del cerebro, quedando retenido en él. El tiempo de vida del Hg2+ en el cerebro es de varios años.[30][29] El mercurio causa neurodegeneración.[31] El Hg0 también cruza la barrera placentaria por lo que accede al sistema nervioso central del feto durante su desarrollo[32] y se incorpora a la leche materna.[33] Una parte del mercurio inhalado es exhalado[25] y otra parte se excreta en la orina y en las heces.[18]
Los iones de mercurio que se incorporan en la saliva son absorbidos en el intestino en un 10%.[29] Algunas bacterias presentes en la flora intestinal y en la saliva pueden metilar el mercurio inorgánico.[34][35] El metilmercurio se absorbe en el intestino en un 90%, cruza la barrera hematoencefálica y es demetilado lentamente en el cuerpo a la forma inorgánica Hg2+.[29]
El mercurio inorgánico Hg2+ tiene una gran afinidad química por los grupos tiol, presentes en algunos aminoácidos azufrados, como la cisteína. La cisteína es una parte estructural de distintas proteínas de membrana, enzimas y de tejidos en los que se acumula el mercurio. La unión del mercurio a estos grupos altera el funcionamiento de muchos procesos normales del cuerpo humano.
Se ha verificado mediante autopsias humanas la existencia de una correlación positiva entre el número de superficies de amalgama en la boca de una persona y la concentración de mercurio inorgánico en distintos tejidos de su cuerpo, especialmente en la glándula pituitaria, la glándula tiroides y la corteza occipital del cerebro.[36] La concentración de mercurio inorgánico en estos tejidos no se correlaciona con la concentración en sangre, orina, cabello o uñas.[36] Las personas portadoras del alelo e4 de la apolipoproteina E tienen una vulnerabilidad mayor a los efectos neurotóxicos del mercurio.[37] En ausencia de tratamiento, la vida media del mercurio en el cerebro humano se aproxima a los 27,4 años.[38]
Opinión de las autoridades sanitarias
editarEn 2008, tras el informe de Maths Berlin al gobierno sueco[39] y la prohibición de los empastes de amalgama en los países escandinavos,[4] el informe del comité SCENIHR de la Comisión Europea ratificó que las amalgamas son un material seguro para la restauración dental.[40] Dicho informe ha recibido duras críticas por parte de toxicólogos.[41] En 2009, pese a tener informes contrarios[42] la FDA también ratificó que la amalgama dental es un material seguro, clasificándola como dispositivo médico clase II.[43] Esta decisión también ha recibido críticas entre toxicólogos.[44]
Referencias
editar- ↑ a b Olsson S, Bergman M. «Daily dose calculations from measurements of intra-oral mercury vapor». J Dent Res. 1992 Feb;71(2):414-23.
- ↑ Ritchie KA. «Mercury vapour levels in dental practices and body mercury levels of dentists and controls». Br Dent J. 2004 Nov 27;197(10):625-32.
- ↑ Chin G, Chong J, Kluczewska A, Lau A, Gorjy S, Tennant M. «The environmental effects of dental amalgam.». Aust Dent J. 2000 Dec;45(4):246-9.
- ↑ a b «Dental Mercury Use Banned in Norway, Sweden and Denmark Because Composites Are Adequate...». Reuters. 3 de enero de 2008. Archivado desde el original el 22 de enero de 2013.
- ↑ Comisión Europea (2012). Study on the potential for reducing mercury pollution from dental amalgam and batteries.
- ↑ Kefi I, Maria A, Majid Z, Sana J, Afreen M, Fareed M, Feroze A, Sajid H, Adel S, Iftikhar A, Yawer A, Kaleem M. «Dental amalgam: effects of alloy/mercury mixing ratio, uses and waste management.». J Ayub Med Coll Abbottabad. 2011 Oct-Dec;23(4):43-5.
- ↑ Norseth J. «Exposure to mercury in public dental clinics in Oslo--an occupational hazard evaluation». Nor Tannlaegeforen Tid. 1977 Sep;87(8):371-6.
- ↑ Ritchie KA, Gilmour WH, Macdonald EB, Burke FJ, McGowan DA, Dale IM, Hammersley R, Hamilton RM, Binnie V, Collington D. «Health and neuropsychological functioning of dentists exposed to mercury.». Occup Environ Med. 2002 May;59(5):287-93.
- ↑ Brune D, Gjerdet N, Paulsen G. «Gastrointestinal and in vitro release of copper, cadmium, indium, mercury and zinc from conventional and copper-rich amalgams». Scand J Dent Res 1983; 91:66-71.
- ↑ Jørgensen K D. «Dentale Amalgamer». Odontologisk Boghandels. Forlag 1976, pp. 63, 141.
- ↑ The physical properties of the silver-tin amalgams. Dent. Cosmos 1896; 38:965.: Black G V. 1986.
- ↑ Alloy for dental amalgam. ISO 1559. First edition. ISO 1559. 1978-11-15.: ISO. 1978.
- ↑ Alloy for dental amalgam. ISO 1559. Second edition. ISO 1559. 1986-06-15.: ISO. 1986.
- ↑ WHO (2003). Elemental mercury and inorganic mercury compounds: Human Health Aspects.
- ↑ Adegbembo AO, Watson PA, Rokni S. «Estimating the weight of dental amalgam restorations». J Can Dent Assoc. 2004 Jan;70(1):30.
- ↑ Weiner JA, Nylander M. «An estimation of the uptake of mercury from amalgam fillings based on urinary excretion of mercury in Swedish subjects.». Sci Total Environ. 1995 Jun 30;168(3):255-65.
- ↑ L Barregård, G Sällsten, and B Järvholm. «People with high mercury uptake from their own dental amalgam fillings». Occup Environ Med. 1995 February; 52(2): 124–128.
- ↑ a b Björkman L, Sandborgh-Englund G, Ekstrand J. «Mercury in saliva and feces after removal of amalgam fillings.». Toxicol Appl Pharmacol. 1997 May;144(1):156-62.
- ↑ IAOMT. «Safe Removal of Amalgam Fillings». Standards of Care Preferred Procedure Approved 9/27/92.
- ↑ Stenman S, Grans L. «Symptoms and differential diagnosis of patients fearing mercury toxicity from amalgam fillings.». Scand J Work Environ Health. 1997;23 Suppl 3:59-63.
- ↑ Langworth S, Strömberg R. «A case of high mercury exposure from dental amalgam.». Eur J Oral Sci. 1996 Jun;104(3):320-1.
- ↑ Sjursen TT, Lygre GB, Dalen K, Helland V, Laegreid T, Svahn J, Lundekvam BF, Björkman L. «Changes in health complaints after removal of amalgam fillings.». J Oral Rehabil. 2011 Nov;38(11):835-48.
- ↑ Wojcik DP, Godfrey ME, Christie D, Haley BE. «Mercury toxicity presenting as chronic fatigue, memory impairment and depression: diagnosis, treatment, susceptibility, and outcomes in a New Zealand general practice setting (1994-2006).». J Oral Rehabil. 2011 Nov;38(11):835-48.
- ↑ Engels P. «Observations on health before and after amalgam removal.». Schweiz Monatsschr Zahnmed. 1998;108(8):811-3.
- ↑ a b Hursh JB, Cherian MG, Clarkson TW, Vostal JJ, Mallie RV. «Clearance of mercury (HG-197, HG-203) vapor inhaled by human subjects.». Arch Environ Health. 1976 Nov-Dec;31(6):302-9.
- ↑ Berglund A, Pohl L, Olsson S, Bergman M. «Determination of the rate of release of intra-oral mercury vapor from amalgam». J Dent Res. 1988 Sep;67(9):1235-42.
- ↑ Snapp KR, Boyer DB, Peterson LC, Svare CW. «The contribution of dental amalgam to mercury in blood». J Dent Res. 1989 May;68(5):780-5.
- ↑ Halbach S, Clarkson TW. «Enzymatic oxidation of mercury vapor by erythrocytes.». Biochim Biophys Acta. 1978 Apr 12;523(2):522-31.
- ↑ a b c d Handbook of the toxicology of metals. En la sección “Mercury” en el capítulo 33, Elsevier, New York, NY, USA, 3rd edition, 2007: M. Berlin, R. K. Zalups, and B. A. Fowler. 2007.
- ↑ Naohiko TAKAHATA M.D., Hideo HAYASHI M.D., Shinya WATANABE M.D., Takeo ANSO M.D. «Accumulation of mercury in the brains of two autopsy cases with chronic inorganic mercury poisoning». Volume 24, Issue 1, pages 59–69, March 1970 DOI: 10.1111/j.1440-1819.1970.tb01457.x.
- ↑ Leong CC, Syed NI, Lorscheider FL. «Retrograde degeneration of neurite membrane structural integrity of nerve growth cones following in vitro exposure to mercury.». Neuroreport. 2001 Mar 26;12(4):733-7.
- ↑ Palkovicova L, Ursinyova M, Masanova V, Yu Z, Hertz-Picciotto I. «Maternal amalgam dental fillings as the source of mercury exposure in developing fetus and newborn.». J Expo Sci Environ Epidemiol. 2008 May;18(3):326-31.
- ↑ Oskarsson A, Schültz A, Skerfving S, Hallén IP, Ohlin B, Lagerkvist BJ. «Total and inorganic mercury in breast milk in relation to fish consumption and amalgam in lactating women.». Arch Environ Health. 1996 May-Jun;51(3):234-41.
- ↑ Rowland IR, Grasso P, Davies MJ. «The methylation of mercuric chloride by human intestinal bacteria». Experientia. 1975 Sep 15;31(9):1064-5.
- ↑ Heintze U, Edwardsson S, Dérand T, Birkhed D. «Methylation of mercury from dental amalgam and mercuric chloride by oral streptococci in vitro.». Scand J Dent Res. 1983 Apr;91(2):150-2.
- ↑ a b Björkman, Lars. «Mercury in human brain, blood, muscle and toenails in relation to exposure: an autopsy study». Environ Health. 2007; 6: 30.
- ↑ Godfrey ME, Wojcik DP, Krone CA. «Apolipoprotein E genotyping as a potential biomarker for mercury neurotoxicity». J Alzheimers Dis. 2003 Jun;5(3):189-95.
- ↑ Rooney, J.P.K. (2014). «The retention time of inorganic mercury in the brain — A systematic review of the evidence». Toxicology and Applied Pharmacology 274 (3): 425-435. doi:10.1016/j.taap.2013.12.011.
- ↑ Maths Berlín (2002). «Mercury in dental-filling materials –– an updated risk analysis in environmental medical terms. An Overview of Scientific Literature published in 1997 to 2002». The Dental Material Commission, Sweden.
- ↑ SCENIHR (2008). The safety of dental amalgam and alternative dental restoration materials for patients and users.
- ↑ Mutter J. «Is dental amalgam safe for humans? The opinion of the scientific committee of the European Commission.». J Occup Med Toxicol. 2011 Jan 13;6(1):2.
- ↑ Bernard Windham (2002). Mercury Exposure Levels from Amalgam Dental fillings; Documentation of Mechanisms by which Mercury causes over 40 Chronic Health Conditions; Results of Replacement of Amalgam fillings; and Occupational Effects on Dental Staff.
- ↑ FDA (2009). Summary of Changes to the Classification of Dental Amalgam and Mercury.
- ↑ OMC (2009). Toxicólogos critican la decisión de la FDA que define la amalgama dental de mercurio como material “seguro”. Archivado desde el original el 29 de septiembre de 2013.